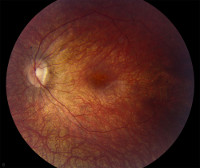
Что такое амавроз?
Амавроз — патология, которая сопровождается резким ухудшением зрения с быстрым его переходом в полную слепоту без видимых причин. Она не связана с болезнью глаз или их повреждением, а вызывается в результате снижения функции зрительного нерва. Есть несколько типов амавроза. Узнаем, каковы их причины и как они лечатся.
Амавроз на сегодняшний день изучен недостаточно. Врачи могут остановить развитие патологии или назначить лечение, но точные причины его возникновения пока неизвестны. Зачастую данный недуг является наследственным, но может быть и приобретенным (преходящим).
Преходящий (транзисторный) амавроз
При этой форме заболевания зрение пропадает временно. Причинами становятся следующие патологии:
При всех этих состояниях нарушается процесс передачи зрительных образов в мозг.
Врожденный амавроз
Его еще называют амаврозом Лебера. При этой патологии выявляются нарушения функций сетчатки. Они начинают развиваться еще в утробе. В сетчатой оболочке родопсин (зрительный пигмент) вырабатывается не полностью, а он отвечает за передачу информации от глаз к мозгу.
Симптомы
Основной симптом — резкая частичная или полная утрата зрения (обратимая и необратимая). Этот признак иногда сопровождается:
Также при амаврозе наблюдаются отеки глазных мышц, боли в глазах, возникают зрительные помехи. Симптомы будут зависеть от причин болезни. Вышеперечисленные признаки сложно определить, когда диагноз нужно поставить ребенку до 3-4 лет, так как он не может описать свое состояние. Врач обращает внимание на такие симптомы, как:
Эти признаки способны заметить и родители. Они должны в этом случае быстрее обратиться к врачу, чтобы избежать осложнений недуга.
Лечение
Лечения амавроза Лебера сегодня не существует. Транзисторную форму можно вылечить путем установления причин болезни и их устранения. Важно вовремя заметить ухудшение зрения и обратиться к специалисту. Самое серьезное осложнение амавроза — полная и необратимая слепота.
Amaurosis fugax что это
В 95% случаев окклюзия центральной артерии сетчатки является следствием тромбоэмболии и рассматривается как форма ишемического инсульта. Приводит к развитию инфаркта сетчатки, который диагностируется по типичной офтальмоскопической картине (позволяет также дифференцировать с кровоизлиянием в сетчатку, в стекловидное тело, с оптической нейропатией). Возможна как окклюзия ствола центральной артерии сетчатки, так и одной из ее ветвей. Типичное клиническое проявление – внезапная безболезненная односторонняя потеря зрения (или выпадение поля зрения). Проявлением ретинальной транзиторной ишемической атаки является преходящая утрата зрения – т.н. amaurosis fugax. Редкой причиной окклюзии артерии сетчатки является артериит. Его своевременное выявление (анамнез, пальпация височной артерии, СОЭ, СРБ) и начало терапии ГКС позволяет сохранить функцию контрлатерального глаза.
При естественном течении заболевания восстановление зрения происходит только в 17% случаев.
Маневры, направленные на снижение внутриглазного давления, перемещение эмбола из центральной артерии в ее ветвь (надавливание на глазное яблоко, пункция передней камеры глаза) не продемонстрировали своей эффективности.
Мета-анализ рандомизированных исследований показал, что применение системного тромболизиса в течение 4,5 часов после появления симптомов увеличивает вероятность восстановления зрения на 50%. Для оценки возможности проведения тромболизиса необходимо выполнение экстренной КТ головного мозга, оценка стандартных противопоказаний. Принципиально возможно выполнение внтуриартериального тромболизиса при наличии опыта у персонала. Иные подходы к консервативной терапии (включая гемодилюцию) неэффективны.
Таким пациентам показана агрессивная вторичная профилактика: модификация факторов риска ССЗ, антиагреганты (если окклюзия криптогенная или вероятно, связана с атеросклерозом), антикоагулянты в случае ФП, решение вопроса о реваскуляроизации в каротидном бассейне в случае наличия выраженного стенозирования.
Mac Grory B, Schrag M, Biousse V, et al. Management of Central Retinal Artery Occlusion: A Scientific Statement From the American Heart Association. Stroke. 2021 Mar 8:STR0000000000000366. doi: 10.1161/STR.0000000000000366. Epub ahead of print. PMID: 33677974.
Рекомендации по ведению пациента с окклюзией центральной артерии сетчатки
Окклюзия центральной артерии сетчатки (ОЦАС) — форма острого ишемического инсульта [1]. Несмотря на более чем 150 лет изучения, нет эффективных доказанных форм терапии этого состояния. Восстановление функциональной остроты зрения в пораженном глазу происходит у менее 20% больных [2,3]. Подобно церебральному ишемическому инсульту, ОЦАС ассоциируется с риском повторных сосудистых событий [4–8].
Дефиниции. ОЦАС — нарушение кровообращения (тромбоэмболия, вазоспазм) в ЦАС или её ветвях с развитием (или без) инфаркта внутренних слоев сетчатки. Диагноз ОЦАС ставится на основании классических клинических данных (внезапная безболевая потеря зрения), нарушении прямой реакции на свет и данных фундоскопии (признаки гипоперфузии сетчатки). При ретинальной транзиторной ишемической атаке (amaurosis fugax) происходит преходящая безболевая монокулярная слепота без резидуальных зрительных нарушений.
Анатомия. Анатомия артериального кровоснабжения глаза представлена на рис. 1.
Рисунок 1. Артериальное кровоснабжение глаза.
Классификация:
— ОЦАС без артериита (95%);
— ОЦАС при артериите (5%, возникает при таких воспалительных заболеваниях, как гигантоклеточный артериит (ГКА)) [9].
Эпидемиология
— 1,9 на 100000 человеко-лет в США [10];
— 1,8 на 100000 человеко-лет в Южной Корее [11];
— 2,5 на 100000 человеко-лет в Японии [12].
Заболеваемость возрастает до 10,1 на 100000 человеко-лет у лиц старше 80 лет [11]. У мужчин заболеваемость немного выше, чем у женщин [11,13].
Этиология
ОЦАС наиболее тесно связана с ипсилатеральным стенозом внутренней сонной артерии (ВСА) [16]. Частота стеноза ВСА ≥70% у пациентов с ОЦАС в исследовании Lavin P. и соавт (2019) составила 37%, в исследовании EAGLE — 40% [17,18]. Другая причина ОЦАС – кардиоаортальная эмболия (фибрилляция предсердий (ФП) — 20%, пороки клапанов — 17%, сердечная недостаточность — 5%) [18]. Согласно исследованию EAGLE у 67% пациентов имеется, по крайней мере, 1 сердечно-сосудистый фактор риска [18]. Более длительный кардиомониторинг связан с более высокой частотой выявления ФП у пациентов с ОЦАС [22]. При этом ОЦАС у пациентов с ФП повышает вероятность повторного инсульта [21]. К редким причинам ОЦАС относятся состояние гиперкоагуляции с тромбозом ЦАС [34] и ятрогенное повреждение (осложнение косметических лицевых инъекций, когда синтетический материал случайно попадает в лицевые артерии, анастомозирующие с глазной артерией) [35].
Диагностика.
— внезапная безболевая монокулярная потеря остроты и периферии зрения (> 80% пациентов имеют остроту зрения «счета пальцев» или хуже). При сохранной цилиоретинальной артерии острота центрального зрения сохранена, но нарушается его периферия.
— снижение прямой реакции на свет, при этом содружественная зрачковая реакция сохранена (если нет контралатеральной оптической нейропатии).
— типичные результаты офтальмоскопии (рис. 2): ретинальный отек (побледнения сетчатки), вишнево-красное пятно (сохраненное хориоидальное кровообращение, окруженное бледностью из-за ишемии сетчатки), медленный сегментарный кровоток в артериях сетчатки, прямая визуализация эмболов ( 50% кислорода поступает в сетчатку за счет пассивной диффузии из хориоидеи, тогда как при ГБО этот показатель достигает 97% [65]. Таким образом, ГБО может принести пользу в качестве временной меры, пока проводится реперфузионная терапия.
Вторичная профилактика
Оптимальный подход – междисциплинарное сотрудничество между неврологом, офтальмологом и терапевтом. Роль офтальмолога – оптимизация остаточной остроты зрения и её динамическая оценка; мониторинг осложнений, связанных с неоваскуляризацией; сохранение здоровья контралатерального глаза. Роль невролога и терапевта – определение причины и начало соответствующей фармакологической стратегии вторичной профилактики (лечение гипертензии, дислипидемии, диабета, ожирения, синдрома обструктивного апноэ сна; отказ от курения; диета; регулярная физическая активность; антитромботическая терапия; хирургическое лечение стеноза ВСА).
У пациентов с NIHSS ≤3 разумно использовать двойную антиагрегантную терапию в течение 21 дня с последующим длительным приемом одного антиагреганта (обычно аспирин 81 мг/сут или клопидогрель 75 мг/сут) [49,72]. При выявлении ФП показан прием антикоагулянтов.
Рисунок 3. Протокол лечения ОЦАС.
Публикации в СМИ
Заболевания сетчатки и зрительного нерва наследственные
Наследственные заболевания сетчатки и зрительного нерва — обширная гетерогенная группа заболеваний, приводящих к снижению или полному отсутствию зрения. В зависимости от преимущественного поражения сетчатки или зрительного нерва выделяют следующие подгруппы.
• Амавроз врождённый — наследуемая абиотрофия палочек и колбочек сетчатки и атрофия зрительных нервов, проявляющиеся быстрым развитием двусторонней центральной скотомы. Наблюдают преимущественно у мужчин, может развиться в любом возрасте (многие формы врождённые — амавроз врождённый Лебера: • тип 1: 204000, GUC2D, GUCSD, LCA1, 600179 [гуанилат циклаза 2D], 17p13; • тип 2: 204100, RPE65 [белок пигментного эпителия сетчатки], 180069, 1p31). Характеризуется прогрессирующим ухудшением зрения. В основе лежат наследуемые заболевания (мутации митохондриального и ядерного геномов). Известно, как минимум, 18 мутаций митохондриальной ДНК и не менее 6 локусов ядерной ДНК. Большую частоту заболевания у мужчин объясняют влиянием андрогенов (например, описан случай резкой потери зрения больным с мутацией MTND4*LHON11778А после терапии андрогенами).
• Атрофия зрительного нерва — конечный результат дистрофических изменений ганглиозных нейронов сетчатки. Первичная атрофия зрительного нерва — генетически обусловленная патология; компонент или единственное проявление при ряде наследственных заболеваний, отличающихся по срокам появления атрофии, степени тяжести, сопутствующим симптомам и типу наследования. Отмечают все основные типы наследования, включая мутации митохондриального генома (атрофия зрительного нерва Лебера, #535000, гены MTND [NADH-убихинон оксидоредуктаза митохондриального генома, КФ 1.6.5.3]).
• Атрофия зрительного нерва — часто компонент наследственных синдромов •• Атаксия Фридрайха с атрофией зрительного нерва и нейросенсорной тугоухостью (136600, Â ) •• Болезнь ван Бухема: иногда первое проявление этой патологии — атрофия зрительного нерва за счёт его сдавления гиперостозными разрастаниями костей черепа •• Атрофия зрительного нерва, глухота и дистальная нейрогенная амиотрофия (258650, r ) •• Метафизарная дисплазия, анетодермия (фокальная атрофия кожи) и атрофия зрительного нерва (250450, r ) •• Атрофия зрительного и слухового нервов с деменцией (311150, À ).
• Дегенерация сетчатки пигментная — прогрессирующая атрофия нейроэпителия с атрофией и пигментной инфильтрацией внутренних слоёв сетчатки. Часто применяемый термин «пигментный ретинит» не совсем точно отражает суть процесса, поскольку воспалительной реакции как таковой не возникает. Основные проявления обусловлены утратой палочек сетчатки. В основе лежит множество мутаций в ряде локусов (например, гены периферина [179605], родопсина [180380], цГМФ управляемого канала фоторецепторов [123825] и др.). Пигментная дегенерация сетчатки, не ассоциированная с другими нарушениями, наиболее часто наследуется как r (268000) и реже как À рецессивная (312600) признак. Доминантное наследование отмечают в 3–4% случаев. Кроме того, атипичный пигментный ретинит наблюдают при множестве других состояний, включая такие рецессивные нарушения, как абеталипопротеинемия (200100), синдромы Альстрема (203800), Рефсума (266500), Барде–Бидла (209900), Лоуренса–Муна (245800), Ашера (276900), Коккейна (216400), паллидарная дегенерация (260200).
• Дегенерация сетчатки коллоидная (сотовидный хориоидит Дойна, *126600, 2p16, ген DHRD, Â ). Множественные очаги округлой формы беловатого цвета, расположенные у диска зрительного нерва и в зоне между верхней и нижней височными артериолами.
• Дистрофия глазного дна Сорсби (#136900, псевдовоспалительная дистрофия глазного дна, 22q12.1–q13.2, ген тканевого ингибитора металлопротеиназы-3 TIMP3 [*188826], Â ). Клинически: дистрофия жёлтого пятна, глазного дна, атрофия сетчатки.
• Дистрофия жёлтого пятна кистозная (*153880, 7p21–p15, ген MDDC, Â ). Клинически: кистозный отёк жёлтого пятна, беловатые точечные отложения в стекловидном теле, дальнозоркость, косоглазие, снижение остроты зрения, перицентральный пигментный ретинит.
• Дистрофия палочек и колбочек, типы и гены: • тип 1, 600624, CORD1, CRD1, 18q21.1 q21.3; • тип 2, 120970, CRX, CORD2, CRD, 602225, 19q13.3
• Дистрофия пигментного эпителия сетчатки, 179605 (мутации гена периферина RDS, RP7), 6p21.1 cen
• Дистрофия сетчатки ранняя (аутосомно рецессивная): 180069, ген RPE65, 1p31
• Дистрофия хориоидеи центральная (215500, ген CACD, 17p)
Дифференциальная диагностика • Инфекционные ретинопатии — вирусные (краснуха) или бактериальные (сифилис) • Остаточные явления экссудативной отслойки сетчатки • Вторичные токсические ретинопатии (хлорохин или фенотиазины) • Другие патологические состояния (окклюзия глазной артерии, травмы).
Течение и прогноз • Прогноз наиболее неблагоприятный при врождённых формах • Течение в большинстве случаев хроническое, медленно прогрессирующее.
МКБ-10 • H31.2 Наследственная дистрофия сосудистой оболочки глаза • H35.5 Наследственные ретинальные дистрофии • Q14 Врождённые аномалии [пороки развития] заднего сегмента глаза
ПРИЛОЖЕНИЯ
Слепота цветовая (ахроматопсия) — отсутствие цветового зрения. Возможность различать любые цвета (трихромазия, основы теории цветного зрения предложил в 1802 г. Томас Янг) определяется присутствием в сетчатке всех трёх зрительных пигментов (для красного, зелёного и синего — первичные цвета). Дихромазии — дефекты цветового восприятия (преимущественно у мужчин; например, разные дефекты у мужчин составляют 8% общей популяции) по одному из первичных цветов — подразделяют на протанопии, дейтанопии и тританопии (от греч. первый, второй и третий [имеются в виду порядковые номера первичных цветов: соответственно красный, зелёный, синий]) • Протанопия (страдает восприятие красного, примерно 25% случаев цветовой слепоты) • Дейтанопия (цветовая слепота по восприятию зелёного, около 75% всех случаев) • Тританопия (страдает преимущественно восприятие фиолетового цвета, дефектное зрение по синему и жёлтому) • Дальтонизм — нарушение цветового зрения — неспособность различать красный и зеленый цвета. МКБ-10. H53.5 Аномалии цветового зрения.
Слепота преходящая (amaurosis fugax) — острый эпизод полной или частичной потери зрения, длящийся обычно не более 10 мин. Причины: кратковременная ишемия в бассейне сонной артерии (как правило, эмболия артерий сетчатки). Лечение • Лекарственная терапия •• Антигипертензивные средства •• Фибринолитические средства •• Антиагреганты (ацетилсалициловая кислота, дипиридамол) • Хирургическое: эндартерэктомия сонной артерии. МКБ-10. G45.3 Преходящая слепота.
Хориоидеремия Х-сцепленная (*303100, ген CHM, Xq21.2; форма с глухотой и ожирением, 303110) — наследственная болезнь глаз, прогрессирующие понижение остроты зрения, сужение полей зрения, гемералопия и близорукость; характерные изменения глазного дна (почти полное отсутствие сосудистого рисунка, резкие контуры и красновато-коричневый цвет жёлтого пятна, нечёткость границ диска зрительного нерва). Синоним: атрофия сосудистой оболочки прогрессирующая. МКБ-10. H31.2 Наследственные дистрофии сосудистой оболочки глаза.
Код вставки на сайт
Заболевания сетчатки и зрительного нерва наследственные
Наследственные заболевания сетчатки и зрительного нерва — обширная гетерогенная группа заболеваний, приводящих к снижению или полному отсутствию зрения. В зависимости от преимущественного поражения сетчатки или зрительного нерва выделяют следующие подгруппы.
• Амавроз врождённый — наследуемая абиотрофия палочек и колбочек сетчатки и атрофия зрительных нервов, проявляющиеся быстрым развитием двусторонней центральной скотомы. Наблюдают преимущественно у мужчин, может развиться в любом возрасте (многие формы врождённые — амавроз врождённый Лебера: • тип 1: 204000, GUC2D, GUCSD, LCA1, 600179 [гуанилат циклаза 2D], 17p13; • тип 2: 204100, RPE65 [белок пигментного эпителия сетчатки], 180069, 1p31). Характеризуется прогрессирующим ухудшением зрения. В основе лежат наследуемые заболевания (мутации митохондриального и ядерного геномов). Известно, как минимум, 18 мутаций митохондриальной ДНК и не менее 6 локусов ядерной ДНК. Большую частоту заболевания у мужчин объясняют влиянием андрогенов (например, описан случай резкой потери зрения больным с мутацией MTND4*LHON11778А после терапии андрогенами).
• Атрофия зрительного нерва — конечный результат дистрофических изменений ганглиозных нейронов сетчатки. Первичная атрофия зрительного нерва — генетически обусловленная патология; компонент или единственное проявление при ряде наследственных заболеваний, отличающихся по срокам появления атрофии, степени тяжести, сопутствующим симптомам и типу наследования. Отмечают все основные типы наследования, включая мутации митохондриального генома (атрофия зрительного нерва Лебера, #535000, гены MTND [NADH-убихинон оксидоредуктаза митохондриального генома, КФ 1.6.5.3]).
• Атрофия зрительного нерва — часто компонент наследственных синдромов •• Атаксия Фридрайха с атрофией зрительного нерва и нейросенсорной тугоухостью (136600, Â ) •• Болезнь ван Бухема: иногда первое проявление этой патологии — атрофия зрительного нерва за счёт его сдавления гиперостозными разрастаниями костей черепа •• Атрофия зрительного нерва, глухота и дистальная нейрогенная амиотрофия (258650, r ) •• Метафизарная дисплазия, анетодермия (фокальная атрофия кожи) и атрофия зрительного нерва (250450, r ) •• Атрофия зрительного и слухового нервов с деменцией (311150, À ).
• Дегенерация сетчатки пигментная — прогрессирующая атрофия нейроэпителия с атрофией и пигментной инфильтрацией внутренних слоёв сетчатки. Часто применяемый термин «пигментный ретинит» не совсем точно отражает суть процесса, поскольку воспалительной реакции как таковой не возникает. Основные проявления обусловлены утратой палочек сетчатки. В основе лежит множество мутаций в ряде локусов (например, гены периферина [179605], родопсина [180380], цГМФ управляемого канала фоторецепторов [123825] и др.). Пигментная дегенерация сетчатки, не ассоциированная с другими нарушениями, наиболее часто наследуется как r (268000) и реже как À рецессивная (312600) признак. Доминантное наследование отмечают в 3–4% случаев. Кроме того, атипичный пигментный ретинит наблюдают при множестве других состояний, включая такие рецессивные нарушения, как абеталипопротеинемия (200100), синдромы Альстрема (203800), Рефсума (266500), Барде–Бидла (209900), Лоуренса–Муна (245800), Ашера (276900), Коккейна (216400), паллидарная дегенерация (260200).
• Дегенерация сетчатки коллоидная (сотовидный хориоидит Дойна, *126600, 2p16, ген DHRD, Â ). Множественные очаги округлой формы беловатого цвета, расположенные у диска зрительного нерва и в зоне между верхней и нижней височными артериолами.
• Дистрофия глазного дна Сорсби (#136900, псевдовоспалительная дистрофия глазного дна, 22q12.1–q13.2, ген тканевого ингибитора металлопротеиназы-3 TIMP3 [*188826], Â ). Клинически: дистрофия жёлтого пятна, глазного дна, атрофия сетчатки.
• Дистрофия жёлтого пятна кистозная (*153880, 7p21–p15, ген MDDC, Â ). Клинически: кистозный отёк жёлтого пятна, беловатые точечные отложения в стекловидном теле, дальнозоркость, косоглазие, снижение остроты зрения, перицентральный пигментный ретинит.
• Дистрофия палочек и колбочек, типы и гены: • тип 1, 600624, CORD1, CRD1, 18q21.1 q21.3; • тип 2, 120970, CRX, CORD2, CRD, 602225, 19q13.3
• Дистрофия пигментного эпителия сетчатки, 179605 (мутации гена периферина RDS, RP7), 6p21.1 cen
• Дистрофия сетчатки ранняя (аутосомно рецессивная): 180069, ген RPE65, 1p31
• Дистрофия хориоидеи центральная (215500, ген CACD, 17p)
Дифференциальная диагностика • Инфекционные ретинопатии — вирусные (краснуха) или бактериальные (сифилис) • Остаточные явления экссудативной отслойки сетчатки • Вторичные токсические ретинопатии (хлорохин или фенотиазины) • Другие патологические состояния (окклюзия глазной артерии, травмы).
Течение и прогноз • Прогноз наиболее неблагоприятный при врождённых формах • Течение в большинстве случаев хроническое, медленно прогрессирующее.
МКБ-10 • H31.2 Наследственная дистрофия сосудистой оболочки глаза • H35.5 Наследственные ретинальные дистрофии • Q14 Врождённые аномалии [пороки развития] заднего сегмента глаза
ПРИЛОЖЕНИЯ
Слепота цветовая (ахроматопсия) — отсутствие цветового зрения. Возможность различать любые цвета (трихромазия, основы теории цветного зрения предложил в 1802 г. Томас Янг) определяется присутствием в сетчатке всех трёх зрительных пигментов (для красного, зелёного и синего — первичные цвета). Дихромазии — дефекты цветового восприятия (преимущественно у мужчин; например, разные дефекты у мужчин составляют 8% общей популяции) по одному из первичных цветов — подразделяют на протанопии, дейтанопии и тританопии (от греч. первый, второй и третий [имеются в виду порядковые номера первичных цветов: соответственно красный, зелёный, синий]) • Протанопия (страдает восприятие красного, примерно 25% случаев цветовой слепоты) • Дейтанопия (цветовая слепота по восприятию зелёного, около 75% всех случаев) • Тританопия (страдает преимущественно восприятие фиолетового цвета, дефектное зрение по синему и жёлтому) • Дальтонизм — нарушение цветового зрения — неспособность различать красный и зеленый цвета. МКБ-10. H53.5 Аномалии цветового зрения.
Слепота преходящая (amaurosis fugax) — острый эпизод полной или частичной потери зрения, длящийся обычно не более 10 мин. Причины: кратковременная ишемия в бассейне сонной артерии (как правило, эмболия артерий сетчатки). Лечение • Лекарственная терапия •• Антигипертензивные средства •• Фибринолитические средства •• Антиагреганты (ацетилсалициловая кислота, дипиридамол) • Хирургическое: эндартерэктомия сонной артерии. МКБ-10. G45.3 Преходящая слепота.
Хориоидеремия Х-сцепленная (*303100, ген CHM, Xq21.2; форма с глухотой и ожирением, 303110) — наследственная болезнь глаз, прогрессирующие понижение остроты зрения, сужение полей зрения, гемералопия и близорукость; характерные изменения глазного дна (почти полное отсутствие сосудистого рисунка, резкие контуры и красновато-коричневый цвет жёлтого пятна, нечёткость границ диска зрительного нерва). Синоним: атрофия сосудистой оболочки прогрессирующая. МКБ-10. H31.2 Наследственные дистрофии сосудистой оболочки глаза.
Амавроз Лебера
Амавроз Лебера – это наследственное заболевание, характеризующееся врожденным поражением светочувствительных клеток сетчатки глаза и в некоторых случаях другими общими нарушениями (аномалии почек, ЦНС). При этой патологии в первые месяцы жизни ребенка или сразу после рождения появляется нистагм, ослабление или отсутствие реакции зрачка на свет. В дальнейшем ребенок может тереть глаза (симптом Франческетти), возникает дальнозоркость и светобоязнь, возможна полная потеря зрения. Диагностика основывается на данных осмотра пациента врачом-офтальмологом, электроретинографии, исследования наследственного анамнеза и генетических анализов. Специфическое лечение амавроза Лебера на сегодняшний день не разработано.
МКБ-10
Общие сведения
Врожденный амавроз Лебера представляет собой гетерогенную группу заболеваний, причиной которых выступают мутации в 18 генах, кодирующих различные белки сетчатки, в том числе опсин. Впервые амавроз был описан еще в XIX веке (в 1867 году) Т. Лебером, указавшим основные проявления этого заболевания – маятниковый нистагм, слепота, появление пигментных пятен и включений на глазном дне. Средняя распространенность заболевания составляет 3:100000 населения.
Амавроз Лебера в равной мере поражает как мужчин, так и женщин. Заболевание составляет примерно 5% от всех наследственных ретинопатий. Современная генетика разрабатывает методики лечения данной патологии, имеются обнадеживающие результаты генной терапии одной из форм амавроза Лебера, обусловленной мутацией в гене RPE65. Отдельно выделяют атрофию зрительных нервов Лебера, которая также характеризуется постепенной потерей остроты зрения и впоследствии полной слепотой. Однако это заболевание совершенно другой генетической природы и обусловлено повреждением митохондриальной ДНК, которая имеет свой уникальный тип наследования (по материнской линии).
Причины
Основной механизм расстройства зрения при амаврозе Лебера – нарушение метаболизма в палочках и колбочках, которое ведет к летальным повреждениям фоторецепторов и их разрушению. Однако непосредственная причина таких изменений различается в зависимости от того, мутация какого именно гена вызвала заболевание.
Один из наиболее распространенных типов амавроза Лебера (тип 2, LCA2) обусловлен наличием мутантного гена RPE65 на первой хромосоме. Известно более 80-ти мутаций этого гена, некоторые из которых, помимо амавроза Лебера, вызывают и определенные формы пигментной абиотрофии сетчатки. Белок, кодируемый PRE65, отвечает за метаболизм ретинола в пигментном эпителии сетчатой оболочки глаза, поэтому при наличии генетического дефекта этот процесс нарушается с развитием побочных метаболических путей. В результате этого синтез родопсина в фоторецепторах прекращается, что и приводит к характерной клинической картине заболевания. Мутантные формы гена наследуются по аутосомно-рецессивному механизму.
Менее распространенная форма амавроза Лебера (тип 14) вызвана мутацией гена LRAT на 4-й хромосоме. Он кодирует белок лецитин-ретинол-ацилтрансферазу, который располагается в микросомах гепатоцитов и обнаружен в сетчатке глаза. Этот фермент участвует в метаболизме ретиноидов и витамина А, из-за наличия мутаций в гене полученный протеин не может полноценно выполнять свои функции, из-за чего развивается дегенерация фоторецепторов, которая клинически проявляется амаврозом Лебера или ювенильной пигментной абиотрофией сетчатки. Имеет аутосомно-рецессивный характер наследования.
Амавроз Лебера тип 8 наиболее часто приводит к врожденной слепоте, ответственный за развитие этой формы заболевания ген CRB1 располагается на 1-й хромосоме и имеет аутосомно-рецессивный характер наследования. При этом выяснено, что кодируемый данным геном белок принимает непосредственное участие в эмбриональном развитии фоторецепторов и пигментного эпителия сетчатки. Более точных данных по патогенезу данной формы амавроза Лебера на сегодняшний день не накоплено. Аналогичная ситуация с мутацией гена LCA5, расположенного в 6-й хромосоме и ассоциированного с 5-м типом амавроза. В настоящее время выявлен только белок, кодируемым данным геном – леберцилин, но его функции в сетчатке непонятны.
Также выявлено две формы амавроза Лебера, которые наследуются по аутосомно-доминантному механизму – тип 7, обусловленный мутацией гена CRX, и тип 11, ассоциированный с нарушением гена IMPDH1. Ген CRX кодирует белок, который обладает множеством функций – контроль развития фоторецепторов в эмбриональный период, поддержание их адекватного уровня во взрослом возрасте, участие в синтезе других протеинов сетчатки (является фактором транскрипции). Поэтому в зависимости от характера мутации гена CRX клиника амавроза Лебера 7-го типа может быть разнообразной – от врожденной слепоты до относительно позднего и вялотекущего ухудшения зрения.
Инозин-5′-монофосфатдегидрогеназа 1, кодируемый геном IMPDH1, представляет собой фермент, регулирующий рост клеток и образование нуклеиновых кислот, однако это пока не позволяет прояснить патогенез того, как нарушения этого белка приводят к 11-му типу амавроза Лебера.
Классификация амавроза Лебера
В настоящее время полностью доказана взаимосвязь между клиническими проявлениями и мутациями определенных генов для 16-ти типов амавроза Лебера. Также имеются указания об открытии еще двух генов, повреждения в которых приводят к такому заболеванию, но пока в этом отношении проводятся дополнительные исследования.
Кроме того, иногда в клинической классификации выделяют не только название поврежденного гена, но и характер мутации, поскольку это имеет значительное влияние на течение амавроза Лебера. Более того, различные типы мутаций в одном и том же гене могут приводить к совершенно разным заболеваниям – например, некоторые разновидности делеций в гене CRX могут приводить не к амаврозу, а к палочко-колбочковой дистрофии. Некоторые мутации генов RPE65, LRAT и CRB1 являются причиной различных форм пигментной абиотрофии сетчатки.
Симптомы амавроза Лебера
Симптоматика амавроза Лебера достаточно вариабельна и зависит от типа заболевания и характера мутации гена. В большинстве случаев при рождении ребенка патология не определяется – даже при осмотре глазного дна изменения наблюдаются лишь в нескольких процентах случаев. По мере его роста родители могут замечать, что ребенок не задерживает взгляд на предметах и окружающих, а в более старшем возрасте может болезненно реагировать на свет (появляется фотофобия), часто тереть глаза и указывать на них пальцем (симптом Франческетти, окулопальцевый синдром). Обнаруживается нистагм, который возникает еще в первые 2-3 месяца жизни и часто является одним из первых проявлений амавроза Лебера, замедленная реакция зрачка на свет или ее полное отсутствие.
В ряде случаев наблюдается врожденная слепота. Если же ребенок родился с относительно сохранной функцией зрения, то в первые годы жизни, помимо указанных симптомов, у его также развивается дальнозоркость, косоглазие, сильно страдает острота зрения. Обычно к 10-ти годам большинство больных с амаврозом Лебера полностью слепнут. В дальнейшем у них могут возникать и другие нарушения зрительного аппарата – кератоконус, катаракта, глаукома. При некоторых типах заболевания могут наблюдаться и сопутствующие нарушения – поражения ЦНС, глухота.
Диагностика
В современной офтальмологии диагностика амавроза Лебера производится на основании осмотра глазного дна, мониторинга динамики изменений в нем, данных электроретинографии. Немаловажную роль играет также изучение наследственного анамнеза, а для некоторых типов заболевания – генетическое секвенирование последовательности ключевых генов.
Дифференциальную диагностику производят с различными формами пигментной абиотрофии сетчатки (при ней сохраняется нормальная или немного сниженная амплитуда волн на электроретинограмме) и некоторыми типами атрофии зрительных нервов.
Лечение амавроза Лебера
На сегодняшний день специфического лечения любого типа амавроза Лебера не существует. На этапе клинических испытаний находится генно-инженерное введение гена RPE65 в сетчатую оболочку глаза больных амаврозом 2-го типа, имеются первые данные о значительном улучшении зрения подопытных больных. В случае же остальных форм заболевания такого прогресса пока нет. Поддерживающее лечение сводится к витаминной терапии, внутриглазным инъекциям сосудорасширяющих средств. При дальнозоркости назначается ношение очков.
Прогноз
В плане сохранения зрения прогноз крайне неблагоприятный, практически 95% больных полностью теряют способность видеть к 10-му году жизни. Кроме того, это наследственное заболевание может осложняться проблемами с ЦНС, почками, эндокринной системой, что требует более тщательного медицинского мониторинга для своевременного выявления подобных нарушений.




_page-0001.jpg)
_page-0001.jpg)