Опыт Резерфорда

Всего получено оценок: 90.
Всего получено оценок: 90.
Важнейшим опытом, демонстрирующим сложное строение атома, стал опыт физика Э. Резерфорда. Рассмотрим суть этого опыта.
Опыт Резерфорда
Модель атома Томсона хорошо описывала явление испускания катодных лучей. Однако, она ничего не говорила о распределении заряда по атому. Для его изучения Э. Резерфорд предложил поставить специальный опыт.
Кратко об опыте Резерфорда можно сказать следующее.
Многие радиоактивные вещества испускают α-частицы, масса которых гораздо больше, чем масса электронов, а заряд равен удвоенному заряду электрона. Теперь, если облучать вещество α-частицами, то легкие электроны, входящие в состав атома, не смогут изменить направление их движения. Рассеяние α-частиц возможно лишь на положительно заряженной части атома.
Экспериментальная установка состояла из контейнера с радием, испускающим α-частицы, на пути частиц ставилась тонкая металлическая фольга, а за фольгой устанавливался экран, покрытый сульфидом цинка, на котором при попадании α-частиц возникало свечение (сцинтилляция). Схема опыта представлена на следующем рисунке:
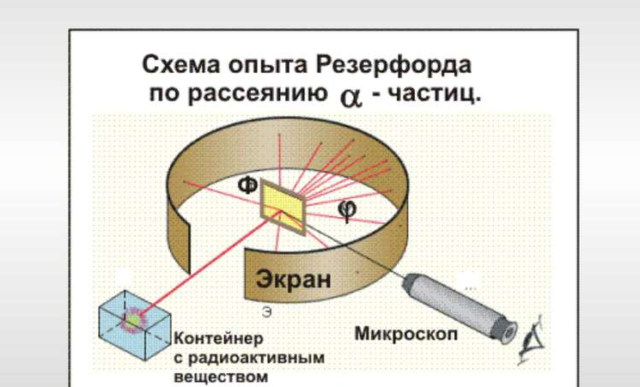
Без фольги, в точке облучения возникало сцинтилляционное пятно. Если на пути полета α-частиц поместить фольгу – размер пятна увеличится за счет рассеяния частиц из-за взаимодействия с положительными зарядами. По характеру изменения пятна можно судить о распределении положительного заряда в атомах вещества.
Результаты опыта
Если положительный заряд равномерно распределен по веществу, рассеяния α-частиц не будет. В соответствии с моделью атома Томсона, положительные заряды имеют некоторую пространственную неоднородность, а значит, рассеяние появится.
Рассеяние, действительно, появилось, но при этом имело довольно интересное распределение – некоторая часть частиц отклонялась на довольно заметные углы, иногда на большие, чем была рассчитана установка.
Это уже говорило о большой неравномерности распределения положительного заряда. Установка была модифицирована, экраны стали устанавливаться вокруг нее.
И с большим удивлением Резерфорд обнаружил, что небольшое число частиц (около 0,05%) отклоняются на очень большие углы, более 90⁰, некоторые – даже «отскакивали» от фольги в обратном направлении.
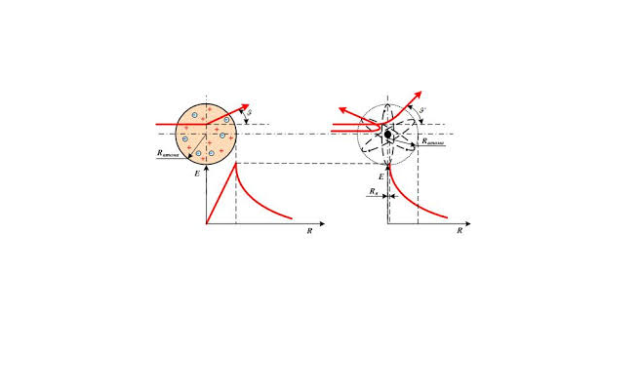
Для такого «отскока» потенциальная энергия электрического отталкивания должна быть равна кинетической энергии α-частицы:
В левой части этой формулы – потенциальная энергия взаимодействия, а в правой – кинетическая энергия частицы.
Опыт Резерфорда также позволяет оценить и заряд ядра. Он оказался разным для разных материалов, и если принять за единицу заряд электрона, то заряд ядра оказался равным порядковому номеру элемента в таблице Менделеева.
Если атом увеличить до размеров орбиты Земли, размер ядра окажется в сто раз меньше, чем размер Солнца.
Что мы узнали?
В опыте Э.Резерфорда по рассеянию альфа частиц поток частиц направлялся на тонкую фольгу, после которой на экране можно было видеть картину рассеяния. Оказалось, что некоторые частицы отклоняются на очень большие углы. Это говорило о том, что положительно заряженный заряд внутри атома сосредоточен в очень малой части атома, которая была названа ядром.
Опыт Резерфорда
Эрнест Резерфорд — уникальный ученый в том плане, что свои главные открытия он сделал уже после получения Нобелевской премии. В 1911 году ему удался эксперимент, который не только позволил ученым заглянуть вглубь атома и получить представление о его строении, но и стал образцом изящества и глубины замысла.
Используя естественный источник радиоактивного излучения, Резерфорд построил пушку, дававшую направленный и сфокусированный поток частиц. Пушка представляла собой свинцовый ящик с узкой прорезью, внутрь которого был помещен радиоактивный материал. Благодаря этому частицы (в данном случае альфа-частицы, состоящие из двух протонов и двух нейтронов), испускаемые радиоактивным веществом во всех направлениях, кроме одного, поглощались свинцовым экраном, и лишь через прорезь вылетал направленный пучок альфа-частиц. Далее на пути пучка стояло еще несколько свинцовых экранов с узкими прорезями, отсекавших частицы, отклоняющиеся от строго заданного направления. В результате к мишени подлетал идеально сфокусированный пучок альфа-частиц, а сама мишень представляла собой тончайший лист золотой фольги. В нее-то и ударял альфа-луч. После столкновения с атомами фольги альфа-частицы продолжали свой путь и попадали на люминесцентный экран, установленный позади мишени, на котором при попадании на него альфа-частиц регистрировались вспышки. По ним экспериментатор мог судить, в каком количестве и насколько альфа-частицы отклоняются от направления прямолинейного движения в результате столкновений с атомами фольги.
Эксперименты подобного рода проводились и раньше. Основная их идея состояла в том, чтобы по углам отклонения частиц накопить достаточно информации, по которой можно было бы сказать что-либо определенное о строении атома. В начале ХХ века ученые уже знали, что атом содержит отрицательно заряженные электроны. Однако преобладало представление, что атом представляет собой что-то похожее на положительно заряженную тонкую сетку, заполненную отрицательно заряженными электронами-изюминами, — модель так и называлась «модель сетки с изюмом». По результатам подобных опытов ученым удалось узнать некоторые свойства атомов — в частности, оценить порядок их геометрических размеров.
Резерфорд, однако, заметил, что никто из его предшественников даже не пробовал проверить экспериментально, не отклоняются ли некоторые альфа-частицы под очень большими углами. Модель сетки с изюмом просто не допускала существования в атоме столь плотных и тяжелых элементов структуры, что они могли бы отклонять быстрые альфа-частицы на значительные углы, поэтому никто и не озабочивался тем, чтобы проверить такую возможность. Резерфорд попросил одного из своих студентов переоборудовать установку таким образом, чтобы можно было наблюдать рассеяние альфа-частиц под большими углами отклонения, — просто для очистки совести, чтобы окончательно исключить такую возможность. В качестве детектора использовался экран с покрытием из сульфида натрия — материала, дающего флуоресцентную вспышку при попадании в него альфа-частицы. Каково же было удивление не только студента, непосредственно проводившего эксперимент, но и самого Резерфорда, когда выяснилось, что некоторые частицы отклоняются на углы вплоть до 180°!
В рамках устоявшейся модели атома полученный результат не мог быть истолкован: в сетке с изюмом попросту нет ничего такого, что могло бы отразить мощную, быструю и тяжелую альфа-частицу. Резерфорд вынужден был заключить, что в атоме большая часть массы сосредоточена в невероятно плотном веществе, расположенном в центре атома. А вся остальная часть атома оказывалась на много порядков менее плотной, нежели это представлялось раньше. Из поведения рассеянных альфа-частиц вытекало также, что в этих сверхплотных центрах атома, которые Резерфорд назвал ядрами, сосредоточен также и весь положительный электрический заряд атома, поскольку только силами электрического отталкивания может быть обусловлено рассеяние частиц под углами больше 90°.
Картина атома, нарисованная Резерфордом по результатам опыта, нам сегодня хорошо знакома. Атом состоит из сверхплотного, компактного ядра, несущего на себе положительный заряд, и отрицательно заряженных легких электронов вокруг него. Позже ученые подвели под эту картину надежную теоретическую базу (см. Атом Бора), но началось всё с простого эксперимента с маленьким образцом радиоактивного материала и куском золотой фольги.
Опыт Резерфорда – кратко о рассеянии альфа-частиц
Важнейшим опытом, демонстрирующим сложное строение атома, стал опыт физика Э. Резерфорда. Рассмотрим суть этого опыта.
Опыт Резерфорда
Модель атома Томсона хорошо описывала явление испускания катодных лучей. Однако, она ничего не говорила о распределении заряда по атому. Для его изучения Э. Резерфорд предложил поставить специальный опыт.
Кратко об опыте Резерфорда можно сказать следующее.
Многие радиоактивные вещества испускают α-частицы, масса которых гораздо больше, чем масса электронов, а заряд равен удвоенному заряду электрона. Теперь, если облучать вещество α-частицами, то легкие электроны, входящие в состав атома, не смогут изменить направление их движения. Рассеяние α-частиц возможно лишь на положительно заряженной части атома.
Экспериментальная установка состояла из контейнера с радием, испускающим α-частицы, на пути частиц ставилась тонкая металлическая фольга, а за фольгой устанавливался экран, покрытый сульфидом цинка, на котором при попадании α-частиц возникало свечение (сцинтилляция). Схема опыта представлена на следующем рисунке:
Рис. 1. Схема опыта Резерфорда по рассеянию альфа частиц.
Без фольги, в точке облучения возникало сцинтилляционное пятно. Если на пути полета α-частиц поместить фольгу – размер пятна увеличится за счет рассеяния частиц из-за взаимодействия с положительными зарядами. По характеру изменения пятна можно судить о распределении положительного заряда в атомах вещества.
Результаты опыта
Если положительный заряд равномерно распределен по веществу, рассеяния α-частиц не будет. В соответствии с моделью атома Томсона, положительные заряды имеют некоторую пространственную неоднородность, а значит, рассеяние появится.
Рассеяние, действительно, появилось, но при этом имело довольно интересное распределение – некоторая часть частиц отклонялась на довольно заметные углы, иногда на большие, чем была рассчитана установка.
Это уже говорило о большой неравномерности распределения положительного заряда. Установка была модифицирована, экраны стали устанавливаться вокруг нее.
И с большим удивлением Резерфорд обнаружил, что небольшое число частиц (около 0,05%) отклоняются на очень большие углы, более 90⁰, некоторые – даже «отскакивали» от фольги в обратном направлении.
Рис. 2. Изменение траекторий альфа частиц при отскоке от ядер.
Для такого «отскока» потенциальная энергия электрического отталкивания должна быть равна кинетической энергии α-частицы:
В левой части этой формулы – потенциальная энергия взаимодействия, а в правой – кинетическая энергия частицы.
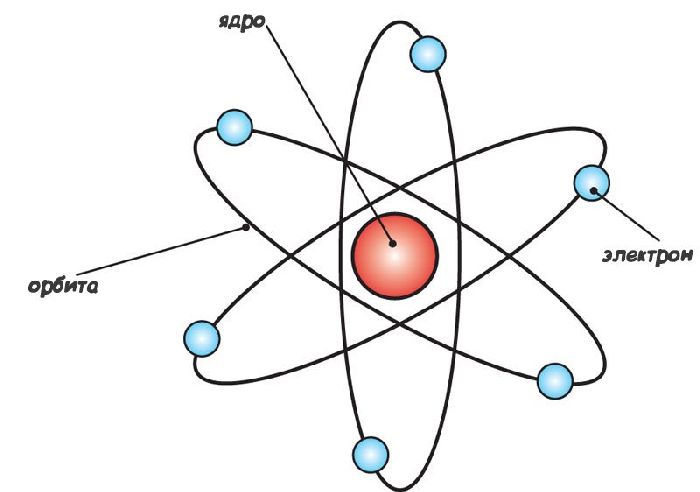
Рис. 3. Планетарная модель атома.
Опыт Резерфорда также позволяет оценить и заряд ядра. Он оказался разным для разных материалов, и если принять за единицу заряд электрона, то заряд ядра оказался равным порядковому номеру элемента в таблице Менделеева.
Если атом увеличить до размеров орбиты Земли, размер ядра окажется в сто раз меньше, чем размер Солнца.
Что мы узнали?
В опыте Э.Резерфорда по рассеянию альфа частиц поток частиц направлялся на тонкую фольгу, после которой на экране можно было видеть картину рассеяния. Оказалось, что некоторые частицы отклоняются на очень большие углы. Это говорило о том, что положительно заряженный заряд внутри атома сосредоточен в очень малой части атома, которая была названа ядром.
Что именно в опыте резерфорда поразило исследователей
На основании исследований Фарадея можно было сделать вывод о существовании внутри атомов электрических зарядов.
Большую роль в развитии атомистической теории сыграл выдающийся русский химик Д. И. Менделеев, разработавший в 1869 году периодическую систему элементов, в которой впервые был поставлен вопрос о единой природе атомов.
Важным свидетельством сложной структуры атомов явились спектроскопические исследования, которые привели к открытию линейчатых спектров атомов. В начале XIX века были открыты дискретные спектральные линии в излучении атомов водорода в видимой части спектра. Впоследствии, в 1885 г. И. Бальмером были установлены математические закономерности, связывающие длины волн этих линий.
В 1896 году А. Беккерель обнаружил явление испускания атомами невидимых проникающих излучений, названное радиоактивностью. В последующие годы явление радиоактивности изучалось многими учеными (, П. Кюри, Э. Резерфорд и др.). Было обнаружено, что атомы радиоактивных веществ испускают три вида излучений различной физической природы (альфа-, бета- и гамма-лучи). Альфа-лучи оказались потоком ионов гелия, – потоком электронов, а гамма-лучи – потоком квантов жесткого рентгеновского излучения.
В 1897 году Дж. Томсон открыл электрон и измерил отношение заряда электрона к массе. Опыты Томсона подтвердили вывод о том, что электроны входят в состав атомов.
Таким образом, на основании всех известных к началу XX века экспериментальных фактов можно было сделать вывод о том, что атомы вещества имеют сложное внутреннее строение. Они представляют собой электронейтральные системы, причем носителями отрицательного заряда атомов являются легкие электроны, масса которых составляет лишь малую долю массы атомов. Основная часть массы атомов связана с положительным зарядом.
Перед наукой встал вопрос о внутреннем строении атомов.
От радиоактивного источника, заключенного в свинцовый контейнер, α-частицы направлялись на тонкую металлическую фольгу. Рассеянные частицы попадали на экран, покрытый слоем кристаллов сульфида цинка, способных светиться под ударами быстрых заряженных частиц. Сцинтилляции (вспышки) на экране наблюдались глазом с помощью микроскопа. Наблюдения рассеянных α-частиц в опыте Резерфорда можно было проводить под различными углами φ к первоначальному направлению пучка. Было обнаружено, что большинство α-частиц проходит через тонкий слой металла, практически не испытывая отклонения. Однако небольшая часть частиц отклоняется на значительные углы, превышающие 30°. Очень редкие α-частицы (приблизительно одна на десять тысяч) испытывали отклонение на углы, близкие к 180°.
Планетарная модель атома, предложенная Резерфордом, несомненно явилась крупным шагом вперед в развитии знаний о строении атома. Она была совершенно необходимой для объяснения опытов по рассеянию α-частиц, однако оказалась неспособной объяснить сам факт длительного существования атома, т. е. его устойчивость. По законам классической электродинамики, движущийся с ускорением заряд должен излучать электромагнитные волны, уносящие энергию. За короткое время (порядка ) все электроны в атоме Резерфорда должны растратить всю свою энергию и упасть на ядро. То, что этого не происходит в устойчивых состояниях атома, показывает, что внутренние процессы в атоме не подчиняются классическим законам.
Опыты Резерфорда
Содержание:
| Предмет: | Физика |
| Тип работы: | Реферат |
| Язык: | Русский |
| Дата добавления: | 06.09.2019 |
Если вам тяжело разобраться в данной теме напишите мне в whatsapp разберём вашу тему, согласуем сроки и я вам помогу!
По этой ссылке вы сможете найти много готовых рефератов по физике:
Посмотрите похожие темы возможно они вам могут быть полезны:
Введение:
Эрнест Резерфорд один из самых известных физиков первой половины 20-го века. Однажды Резерфорд первым расчленил атом, обнаружив в нем ядро. Он исследовал сложные явления, происходящие в этой поразительно маленькой частице материи, а затем в своей лаборатории он расщепил ядра атомов.
Еще будучи студентом 2 курса Университета Резерфорда, на одной из конференций он выступил с докладом на тему «Эволюция элементов». Резерфорд предположил, что все химические элементы представляют собой сложные химические системы, состоящие из одинаковых элементарных частиц. В то время атом считался неделимым в физике доминировала теория неделимости атомов Дальтона.
Опыты Резерфорда
Первая попытка создания атомной модели на основе накопленных экспериментальных данных принадлежит Дж. Томсон. По мнению Томсона, электроны вкраплены в сверхминиатюрную сферу диаметром 10–8 см, в которой положительные заряды распределены равномерно. Вместе с отрицательно заряженными электронами сфера электрически нейтральна. Это атом. В то время Резерфорд, который работал в одной лаборатории с Томсоном, так и думал и даже не мечтал, что сможет создать более совершенную модель, основанную на новых идеях.
В 1896 году А. Беккерель, изучая свечение различных веществ, случайно обнаружил, что соли урана выделяются без предварительного освещения. Это излучение обладает большой проникающей способностью и способно воздействовать на фотопластинку, завернутую в черную бумагу. Резерфорд немедленно начал изучать лучи Беккереля. Он начал свое исследование рентгеновских лучей, проверив свою гипотезу о связи между рентгеновскими лучами и лучами Беккереля. Эта идея пришла ему в голову по очень простой причине: они оба произвели ионизацию воздуха. Эта идея была неудачной.
Резерфорд обнаружил эманацию тория и доказал, что этот радиоактивный газ, выпущенный из тория, является химическим элементом, отличным от самого тория. Позже он определил атомный вес эманации и показал, что это благородный газ нулевой группы системы Д.И. Менделева.
После этого Резерфорд вместе с Гейгером и Марсденом провел новую серию экспериментов. Результаты произвели революцию в физике. Это была самая драматичная глава в науке нашего времени. Резерфорд открыл атомное ядро и основал новую чрезвычайно важную науку ядерную физику.
Доверив Марсдену эту работу, Резерфорд не ожидал найти ничего интересного. При условии, что модель атома Томсона верна (и тогда нет оснований сомневаться в этом), эксперимент должен был показать, что частицы свободно проходят через металлические препятствия. Однако что-то все же заставило Резерфорда предпринять этот новый эксперимент.
Новый рост гения Резерфорда
На основании этих исследований Резерфорд предложил ядерную (планетарную) модель атома. Согласно этой модели, вокруг положительного ядра, имеющего заряд ze (z порядковый номер элемента в системе Менделеева, e элементарный заряд), размер составляет 10-15 10-14 м, а масса практически равна к массе атома, в области с линейными размерами порядка 10-10 м по замкнутым орбитам движутся электроны, образуя электронную оболочку атома. Поскольку атомы нейтральны, заряд ядра равен общему заряду электронов, т.е. z-электроны должны вращаться вокруг ядра.
Для простоты будем считать, что электрон движется вокруг ядра по круговой орбите с радиусом r. В этом случае кулоновская сила взаимодействия между электроном и ядром придает электрону центростремительное ускорение. Второй закон Ньютона для электрона, движущегося по кругу под действием кулоновской силы, имеет вид, где me и v масса и скорость электрона на орбите радиуса r, электрическая постоянная.
Попытки построить модель атома в рамках классической физики не привели к успеху: модель Томсона была опровергнута экспериментами Резерфорда, а модель ядра оказалась электродинамически нестабильной и противоречила экспериментальным данным. Преодоление возникших трудностей потребовало создания качественно новой квантовой теории атома.
В 1914 году началась Первая мировая война, и Резерфорду пришлось на некоторое время отложить свои исследования. Но периодически, работая на военную промышленность, он возвращался к собственным экспериментам. В своих следующих экспериментах Резерфорд планировал взломать атом.
Эти попытки увенчались полным и огромным успехом. Новый рост гения Резерфорда привел к открытию, которое впоследствии произвело революцию во всей науке и технике нашего времени. Первый сигнал был дан для начала атомного века. Резерфорд расколол атомное ядро.
Идея этого возникла в Резерфорде при наблюдении в камере Вильсона (к тому времени она уже была изобретена и улучшена) и в сцинтилляционном счетчике таинственных следов (следов), намного длиннее следов; частицы, хорошо известные ему по бесчисленным экспериментам. Он думал, что есть некоторые неизвестные причины для резкого увеличения диапазона частиц. Другое предположение (оно оказалось верным) состоит в том, что другие неопознанные частицы оставляют длинные следы. Перед исследователем стояла задача выяснить, какое из двух предположений является верным.
Чтобы получить ответ на свои вопросы, Резерфорд решил провести серию экспериментов по бомбардировке частицами различных веществ. Он построил устройство, которое сейчас кажется нам необычайно простым. Но мы также должны признать, что только он был наиболее подходящим для визуального решения проблемы. В нем мишенями для бомбардировки должны были быть газы (то есть легкие атомы), а не металлические пластины, обычно используемые Резерфордом во многих предыдущих экспериментах.
Устройство, фактически построенное Резерфордом, с помощью которого он первым разделил ядра атомов легких элементов, схематично показано на рисунке.
Когда Резерфорд наполнил трубку азотом, в поле зрения появились частицы, оставив очень длинный след, подобный тому, что он уже наблюдал. Конечно, Резерфорд провел еще много экспериментов, прежде чем прийти к окончательным выводам. Но окончательный вывод был такой: при столкновении; частицы с ядрами азота, некоторые из этих ядер разрушаются, испуская ядра водорода протоны, а затем образуется ядро кислорода.
Колоссальное значение этого открытия с самого начала было ясно самому Резерфорду и его сотрудникам. Деление атомных ядер было проведено впервые. Непоколебимая, как казалось раньше, идея «неразрывности» химических элементов была явно опровергнута. Открылись совершенно новые и удивительные возможности искусственного производства одних элементов из других, высвобождения огромной энергии, содержащейся в ядрах и т. д.
Заключение
В результате длительных экспериментов Резерфорд смог вызвать ядерные реакции в 17 легких элементах.
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.







