Синокром, Ферматрон, Нолтрекс: сравнение препаратов
Назначая пациентам внутрисуставные инъекции заменителя синовиальной жидкости, многие врачи традиционно рекомендуют препараты, которые у всех на слуху. К таковым относятся, к примеру, «Ферматрон» и «Синокром» – лекарства на основе гиалуроната натрия.
Агрессивный маркетинг сделал свое дело: сегодня люди больше доверяют рекламе, чем здравому смыслу. А между тем есть у этих популярных препаратов и обратная сторона. В чем принципиальная разница между «Ферматроном», «Синокроном» и синтетическим эндопротезом «Нолтрекс»? О чем умалчивают производители?
Сравнение характеристик препаратов «Ферматрон», «Синокром» и «Нолтрекс»
Синокром
Ферматрон
Нолтрекс
1 % раствор гиалуроната натрия
1 % или 1,5 % раствор гиалуроната натрия
4,5 % раствор искусственного биополимера
Количество инъекций на курс
После какой по счету инъекции наступает улучшение
Количество инъекций при тяжелом течении остеоартроза
Продолжительность эффекта при средней и умеренной степени тяжести остеоартроза
Скорость выведения из организма
Способность вызывать аллергию
остеоартроз умеренной и средней степени тяжести
остеоартроз умеренной и средней степени тяжести
остеоартроз любой степени тяжести
Локальные явления после введения (покраснение, боль)
Продолжительность побочных эффектов
«Крома Фарма ГмбХ» (Австрия)
Hyaltech Ltd (Великобритания)
Как долго сохраняется эффект
Главное отличие между препаратами – продолжительность эффекта после инъекций, а также период от начала курса лечения, после которого заметен результат (снижается боль).
Препараты на основе гиалуроновой кислоты – «Ферматрон», «Синокром» – производятся с применением технологии автоклавирования. Под действием высоких температур молекулы быстро распадаются, поэтому для достижения эффекта необходимо пройти курс из нескольких инъекций, в среднем до пяти. Результат заметен не сразу, а только спустя 2-3 недели, то есть после второй-третьей процедуры – в зависимости от степени тяжести заболевания. После первой процедуры зачастую улучшений не наступает, и пациент только жалуется на побочные явления – дискомфорт в месте введения.
«Нолтрекс» – препарат синтетического происхождения для лечения остеоартроза, который отличается высокой стойкостью молекул к распадам. Попадая внутрь сустава, он остается там надолго, чем и объясняется его продолжительный эффект, а также почти моментальное действие. Заметное облегчение болевого синдрома наступает уже после первой инъекции этого искусственного заменителя синовиальной жидкости. В чем секрет?
Чтобы ушла боль, нужно сделать 3 инъекции «Ферматрон»
Молекулярная масса препаратов: почему об этом надо знать
Молекулярная масса – это та информация, которую производители многих эндопротезов синовиальной жидкости намеренно умалчивают. Вместо нее – подаются различные маркетинговые сведения об инъекциях гиалуроновой кислоты, часто не подкрепленные фактами.
Взглянем на проблему с научной точки зрения. Препараты с высокой молекулярной массой имеют множественные межмолекулярные поперечные связи. Чтобы эндопротез рассосался в суставе, они должны нейтрализоваться – молекулы постепенно распадаются и выводятся из организма. Чем выше молекулярная масса препарата, тем более долгим у него будет период распада молекул, а значит, лекарство сохранится внутри сустава дольше. В аналогах с низкой молекулярной массой (в их числе – «Ферматрон», «Синокром») этот процесс происходит очень быстро, поэтому человек вынужден снова и снова отправляться на процедуру.
Главная задача жидких эндопротезов, будь то «Ферматрон» или «Нолтрекс», – как можно дольше находиться в суставной сумке, покрывать поврежденные хрящи и предупреждать их трение. Чем дольше они остаются в суставе, тем дольше человек с диагнозом «остеоартроз» не испытывает боли во время движений. Этот период напрямую зависит не от названия препарата и не от дозировки гиалуроновой кислоты, и даже не от страны-производителя: значение имеет только молекулярная масса.
Препараты на основе гиалуроновой кислоты «Ферматрон» и «Синокром» имеют молекулярную массу соответственно 1 и 1,6 млн Да. Молекулярная маса Noltrex составляет более 10 млн Да, то есть синтетический заменитель синовиальной жидкости рассасывается и выводится из организма почти в 10 раз дольше! Этим и объясняется его более продолжительный эффект – до двух лет, а также быстрый результат – уже после первой инъекции.
«Нолтрекс» – единственный препарат на рынке с высокой молекулярной массой (более 10 млн Да)
Цена лечения препаратами «Синокром», «Ферматрон» и «Нолтрекс»
«Синокром» – раскрученный, брендовый, импортный препарат. Его средняя цена за инъекцию – 6400 руб. (по состоянию на четвертый квартал 2018 г.) Курс включает 3-5 уколов с недельным интервалом, то есть общая стоимость лечения составит 19-32 тыс. руб. Уже через полгода его придется повторить, то есть затраты на лечение остеоартроза составят 38-64 тыс. рублей в год.
«Синокром» – очень дорогой жидкий эндопротез
«Ферматрон» – еще один известный, широко разрекламированный препарат гиалуроновой кислоты с низкой молекулярной массой. Препарат 1 % раствора стоит 4400 руб. (раствор гиалуроната натрия 1,5 % – около 6 тыс. руб.). Курс лечения включает 3-4 инъекции, что эквивалентно 13-17,5 тыс. руб. Уже спустя полгода курс придется повторить, то есть стоимость годового лечения остеоартроза «Ферматроном» составит 26-35 тыс. руб.
«Нолтрекс» – синтетический заменитель синовиальной жидкости российского производства, который реализуется по более низкой цене за счет лояльной маркетинговой политики. Стоимость препарата – 3100 руб. Курс лечения включает 1-3 инъекции, то есть обойдется не более чем 9300 руб.
Эндопротез действует гораздо дольше, чем полгода, – до 18-24 месяцев, за счет высокой молекулярной массы. Поэтому повторно проходить курс придется каждые полтора-два года (в тяжелых случаях этот период может сокращаться до 9-12 месяцев). Стоимость лечения остеоартроза в год составит не более 9300 руб., а если эту сумму разделить на полтора-два – и того меньше!
Лечить остеоартроз инъекциями «Нолтрекс» обходится дешевле, чем «Ферматроном», в 2,5-3,5 раза
Многие ортопеды-ревматологи по привычке назначают пациентам раскрученные жидкие эндопротезы, которые у всех на слуху. Мы привыкли доверять врачам, поэтому редко задаемся вопросами, почему фигурирует именно это лекарство, и уж тем более не спорим. Не каждому человеку с диагнозом «остеоартроз» везет попасть к прогрессивному специалисту, который объяснит разницу между гиалуроновой кислотой и синтетическими препаратами. А между тем разница очевидна!
Лечение артроза заменителем синовиальной жидкости «Нолтрекс» – более эффективно, чем препаратами на основе гиалуроната натрия «Ферматрон» и «Синокром». Причина – в высокой молекулярной массе и искусственном происхождении лекарства. Не стоит упускать из виду и финансовый аспект: с Noltrex можно сэкономить львиную долю семейного бюджета.
Сравнительная эффективность курсовой инъекционной терапии Инъектраном или в комбинации с Ферматроном у пациентов с остеоартритом голеностопных суставов на фоне базового приема Генитрона
Опубликовано в журнале:
« Эффективная фармакотерапия » № 23, 2019
Ключевые слова: остеоартрит, голеностопный сустав, хондропротекторы, нестероидные противовоспалительные препараты, хондроитина сульфат, гиалуроновая кислота, мелоксикам
Comparative Efficacy of the Course Injection Therapy with Iniectran or in Combination with Fermathron in Patients with Osteoarthritis of the Ankle Joints on the Background of Genytron Basic Application
Key words: osteoarthritis, ankle joint, chondroprotectors, nonsteroidal anti-inflammatory drugs, chondroitin sulfate, hyaluronic acid, meloxicam
Введение
Несмотря на высокую медико-социальную значимость заболевания, стандартов оказания помощи при поражении голеностопного сустава не существует. Действующий стандарт по оказанию помощи больным артрозами 2005 г. предписывает использовать нестероидные противовоспалительные препараты (НПВП) и глюкокортикостероиды (ГКС). При этом этиопатогенетическая терапия не предлагается [4].
Материал и методы
Таблица 1. Общая характеристика больных, включенных в исследование
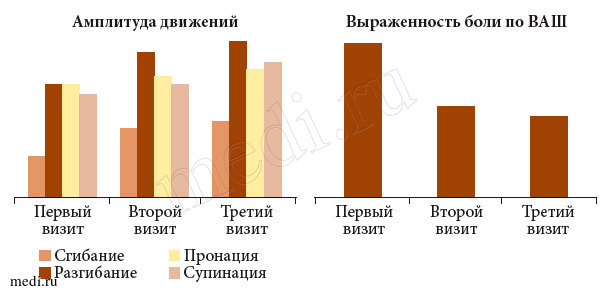
Все больные успешно прошли курс назначенной терапии. Изменение показателей эффективности лечения у пациентов первой группы представлено на рис. 1. У большинства получавших Инъектран амплитуда сгибания и разгибания во время второго визита статистически значимо увеличилась (p > 0,1). Степень боли уменьшилась на 25 мм к моменту второго визита (p > 0,1). В отличие от первой группы динамика морфологических изменений была статистически значимой (p > 0,10
> 0,10
Рис. 2. Динамика изучаемых показателей во второй группе на фоне лечения
Сравнение результатов лечения в первой и второй группах показало, что применение исследуемых препаратов было эффективным. Однако совместное использование Инъектрана и Ферматрона на фоне базового приема Генитрона обеспечивало синергизм лечебного воздействия, о чем свидетельствует динамика клинических и параклинических показателей. В третьей группе также наблюдалась положительная динамика оцениваемых показателей. Однако в отношении большинства из них не отмечено статистической достоверности результатов, за исключением выраженности боли и синовита во время второго визита. Как и в первой группе, указанные показатели ухудшились к третьему визиту (рис. 3, табл. 6).
Таблица 5. Динамика клинических и лабораторных показателей эффективности терапии во второй группе
Обсуждение результатов
Заключение
На амбулаторном этапе среди пациентов с начальными стадиями ОА голеностопного сустава следует выделять когорту с преобладанием в клинической картине фазы обострения по типу артритической. Таковая характеризуется стойким синовитом и изменением лабораторных показателей, ассоциированных с воспалением. Использование в качестве комплексного консервативного лечения ОА голеностопного сустава препаратов Инъектран, Ферматрон и Генитрон достоверно позволяет добиться раннего клинического ответа. Причиной достижения значимых показателей может быть взаимодействие хондроитина сульфата и гиалуроновой кислоты. В частности, хондроитина сульфат защищает гиалуроновую кислоту от воздействия гиалуронидазы и аггрекиназы путем угнетения их активности и потенцирования противовоспалительного действия, а также регуляторного эффекта на метаболизм хряща. При определении выраженности эффекта предложенной схемы амбулаторного лечения ОА голеностопного сустава первой и второй степени оценка синовита и лабораторных показателей воспаления была значимой, но не всегда статистически доказательной. Полученные результаты позволяют рекомендовать предложенную схему терапии (хондроитина сульфат плюс гиалуроновая кислота плюс мелоксикам) для включения в регламентирующие документы по лечению больных ОА голеностопных суставов при условии получения достаточной доказательной базы.
Современные тенденции в лечении остеоартрита. Внутрисуставное применение производных гиалуроновой кислоты

Статья представляет собой подробный разбор механизмов действия производных гиалуроновой кислоты для внутрисуставной терапии остеоартрита, включающий в себя сравнительную оценку различных характеристик средств данной группы, таких как эластичность, упругос
The article presents detailed analysis of action mechanisms of hydraulic acid derivatives for intra-articular therapy of osteoarthritis, which includes comparative assessment of different characteristics of preparations from this group, such as elasticity, resilience, molecular mass. Special attention is paid to synovial liquid prostheses.
Остеоартрит (ОА) в настоящее время занимает ведущее место по распространенности среди хронических дегенеративных заболеваний суставов и вызывает инвалидизацию миллионов людей во всем мире. По официальным данным, за 2011 г. только в России это заболевание было выявлено у 3 млн 700 тыс. человек, причем прирост данного заболевания составляет 745 тыс. человек за год. И эта статистика охватывает лишь тех людей, которые официально обратились за медицинской помощью, реальная же ситуация гораздо более печальная: данные эпидемиологических исследований показывают, что распространенность ОА в нашей стране выше более чем в 4 раза и составляет порядка 15 млн человек.
Данная проблема значительно осложняется тем, что существующие сегодня методики лечения ОА, как правило, не приводят к желаемым результатам. В настоящее время широкое развитие получили оперативные пути лечения, такие как эндопротезирование суставов, проводимое на поздних стадиях заболевания, остеотомии костей с изменением осей нагрузки на конечности, выполняемые при частичном поражении опорных суставов, малоинвазивные артроскопические методики замещения суставного хряща при локальных его дефектах. Однако все эти методы имеют и свои отрицательные стороны — это, как правило, непростой реабилитационный период, интраоперационные риски, особенно учитывая то, что контингент больных с ОА составляют главным образом пациенты пожилого и старческого возраста с большим количеством сопутствующих соматических заболеваний. Поэтому одной из важнейших задач современной медицины является улучшение качества жизни пациентов с этой тяжелой, хронической, постоянно прогрессирующей патологией консервативным путем.
В настоящее время в рамках медикаментозной терапии ОА существует несколько направлений, которые рекомендуется использовать в комплексе. Это в первую очередь нестероидные противовоспалительные препараты различных видов (селективные и неселективные ингибиторы ЦОГ-1 и ЦОГ-2), которые имеют ряд серьезных противопоказаний со стороны желудочно-кишечного тракта и сердечно-сосудистой системы и должны назначаться с особой осторожностью с учетом всех существующих рисков. Также широко применяются препараты хондропротекторного ряда, имеющие в своем составе хондроитин сульфат и глюкозамин сульфат, однако их эффективность при применении в формате монотерапии вызывает большое сомнение, и данная группа препаратов должна использоваться в качестве дополнения к основному лечению.
Основой лечения ОА, безусловно, является работа с мышечно-связочным аппаратом суставов, так как в большинстве случаев резкое прогрессирование данного заболевания происходит именно по причине слабости стабилизирующего комплекса пораженного сустава. В связи с этим любая медикаментозная терапия будет недостаточно эффективна, если не уделять внимание регулярной лечебной физической культуре, которая должна проводиться под контролем врача с учетом кинезиологических особенностей каждого конкретного пациента.
Особое место в терапии ОА занимают инъекцонные внутрисуставные формы препаратов. Это и препараты кортикостероидов, которые обладают значительным противовоспалительным эффектом, однако очень негативно влияют на структуру суставного хряща, провоцируя в дальнейшем прогрессирование дегенеративных процессов в суставе. Это также препараты плазмы, обогащенной тромбоцитами, которые оказывают положительное влияние как на поврежденные участки суставного хряща, так и на внутрисуставную среду в целом, однако при выраженных дегенеративных изменениях в суставе их эффективность невысока, применение данных препаратов скорее оправданно при локальных свежих посттравматических дефектах суставного хряща.
Золотым стандартом лечения ОА является внутрисуставное введение препаратов гиалуроновой кислоты, одного из важнейших компонентов суставного хряща, которые уменьшают симптомы заболевания уже в течение первой недели с начала терапии и сохраняют свой эффект длительное время. Современная медицина в настоящий момент обладает достаточно большим спектром препаратов на основе гиалуроновой кислоты, имеющих различия по многим параметрам, таким как концентрация, молекулярный вес, методика производства. У пациентов с ОА в синовиальной жидкости снижены концентрация и средний молекулярный вес гиалуронатов. Это в первую очередь послужило исходным обоснованием для применения внутрисуставных инъекций гиалуроновой кислоты в клинической практике [2]. В дальнейшем были исследованы как гиаладгерины (отвечают за образование поперечных сшивок у гиалуронанов в синовиальной жидкости и внеклеточном хрящевом матриксе), так и рецепторы гиалуронатов на поверхности клеток [3]. Сообщалось, что эластичность и способность поддерживать работоспособность сустава для экзогенных гиалуронатов тем выше, чем выше молекулярная масса [4]. Этот факт породил гипотезу, что длительность клинического эффекта от гиалуронатов также пропорциональна молекулярной массе в результате повышения вязкости (механические и смазочные функции), продолжительности нахождения в суставе и стимуляции синтеза эндогенных гиалуронатов. Однако результаты клинических испытаний, в которых сравнивались гиалуронаты с различным молекулярным весом, показывают, что влияние на патогенез и прогрессию ОА наблюдается для всего спектра протестированных молекулярных масс.
Важными характеристиками свойств препаратов гиалуроновой кислоты являются вязкость и упругость. Упругость зависит от сдвига: механические свойства гиалуронатов изменяются в зависимости от приложенного усиления сдвига и скорости потока. Раствор гиалуронатов ведет себя как вязкая жидкость, когда внешние силы действуют на низких скоростях, и как эластичное тело, когда подвергается действию повышенных сил или высоких скоростей. Таким образом, гиалуронаты являются эффективным смазочным средством при медленных движениях и прекрасными амортизаторами при быстрых движениях [4].
Очевидно, что такое упругое поведение в значительной степени влияет на клинические проявления, но фармакокинетический профиль гиалуронатов указывает, что роль этих субстанций не ограничивается чисто механической. В ходе движений гиалуронаты попадают в лимфатическую систему суставной капсулы, далее в общий кровоток и в итоге абсорбируются печенью, где деградируют до воды и углекислого газа [6]. Длительность терапевтического эффекта гиалуронатов, как показывают клинические испытания, также не соотносится с их чисто механической ролью, поскольку положительный эффект сохраняется в течение нескольких месяцев после проведения курса инъекций, хотя период полувыведения гиалуронатов из суставов составляет несколько часов или дней [7, 8].
Большое значение имеют данные об увеличении упругих свойств синовиальной жидкости после экзогенного введения гиалуроновой кислоты. Mensitieri и Ambrosio проанализировали синовиальную жидкость из коленного сустава пациентов после пункции сустава или лечения с помощью гиалуронатов. Упругость синовиальной жидкости у пациентов, получавших гиалуронаты, была повышена как относительно первоначальных показателей (до лечения), так и относительно пациентов, перенесших пункцию сустава. Повышенная упругость наблюдалась в течение одной недели после инъекций; к этому времени экзогенное вещество уже должно было вывестись из суставной сумки. Этот факт свидетельствует, что упругость синовиальной жидкости находится в положительной зависимости как от концентрации гиалуроновой кислоты, так и от молекулярной массы молекулы.
Основными характеристиками вязкоупругих свойств раствора гиалуроновой кислоты являются модуль упругости, или модуль накопления (G’), и модуль вязкости, или модуль потерь (G»). В первую очередь при патологии сустава снижаются эластические свойства (модуль упругости), поэтому пациент может хорошо переносить только небольшие нагрузки. Происходит также повышение частоты пересечения кривых модуля упругости и модуля вязкости, то есть момента, когда свойства синовиальной жидкости изменяются с преимущественно вязких на преимущественно упругие.
В статье E. A. Balazs (1974) приведены данные о точке пересечения модулей у людей разных возрастов (табл. 1), которая показывает, что с возрастом даже у здоровых происходит некоторое увеличение значения точки пересечения модулей.
На рис. (A. Madkhali и соавт., 2016) изображена зависимость модуля вязкости и модуля упругости синовиальной жидкости здоровых добровольцев, пациентов с воспалительно-дегенеративными заболеваниями суставов, а также модуля вязкости и упругости раствора гиалуроновой кислоты от нагрузки. Обнаружено, что синовиальная жидкость здоровых добровольцев характеризуется высоким модулем вязкости при малой нагрузке (0,5 Гц) и высоким модулем упругости при большой нагрузке (2,5 Гц). Частоты 0,5 Гц и 2,5 Гц были выбраны не случайно, так как в модельных системах они отражают нагрузку на сустав при ходьбе (0,5 Гц) и при беге (2,5 Гц).
Исходя из этих данных, для обеспечения оптимальной эффективности препарата гиалуроновой кислоты в суставе необходимо, чтобы перекрест кривых модуля вязкости (G’) и модуля упругости (G») происходил в диапазоне частоты от 0,5 Гц до 2,5 Гц.
Современными средствами для замещения синовинальной жидкости в суставах являются Рипарт и Рипарт Лонг, производимые на основе гиалуроновой кислоты по запатентованной швейцарской технологии в России. Они производятся методом бактериальной ферментации Streptococcus equi и Streptococcus zooepidеmiсus. Уникальная технология производства позволила сократить время приготовления раствора с 24 часов до 30 минут, время стерилизации с 60 до 30 минут, а также производить двойную ультрафильтрацию через фильтр с диаметром пор 5 мкм, что в свою очередь позволило сократить длительность повреждающего термического воздействия, добиться полной денатурации гиалуронидазы и лучшей очистки продукта от белковых включений. В конечном итоге удалось снизить риск содержания бактериальных эндотоксинов, полностью очистить раствор от гиалуронидазы, повысить однородность, снизить вариативность вязкоэластичных характеристик средства для замещения синовинальной жидкости от серии к серии, а также сохранить его молекулярную массу. Молекулярная масса Рипат и Рипарт Лонг составляет не менее 3 млн Да, данный показатель является уникальным для средств, полученных процессом ферментации, и обеспечивает оптимальное взаимодействие с суставным хрящом пораженных ОА суставов.
В настоящее время общепризнанной является точка зрения, согласно которой гиалуронаты с максимально близкими к здоровой синовиальной жидкости человека свойствами обеспечивают наилучшую защиту суставного хряща. Синовиальная жидкость здорового человека характеризуется перекрестом кривых модуля вязкости (G’) и модуля упругости (G») в диапазоне частоты нагрузки 0,5–2,5 Гц и значением модуля упругости и модуля вязкости не менее 5 Па при 0,5 Гц, не менее 7 Па при 1 Гц. Данные, приведенные в табл. 2, наглядно показывают, что Рипарт и Рипарт Лонг полностью соответствуют вышеуказанным критериям.
Также немаловажным преимуществом Рипарт и Рипарт Лонг является то, что существует большой ассортимент форм выпуска: 2 дозировки 10 мг/мл (Рипарт) и 20 мг/мл (Рипарт Лонг), каждая дозировка в трех формах выпуска: 1, 2 и 3 мл, чего нет практически ни у одного производителя данной продукции. Основываясь на опыте применения Рипарт и Рипарт Лонг, необходимо особо отметить, что не зафиксировано практически ни одного случая воспалительных осложнений в суставах после введения, что говорит о высоком профиле безопасности. Все приведенные выше данные позволяют с уверенностью утверждать, что Рипарт и Рипарт Лонг являются одними из наиболее безопасных и эффективных производных гиалуроновой кислоты в лечении ОА.
Литература
А. И. Найманн, кандидат медицинских наук
ООО «Клиника Экспертных Технологий», Москва
Современные тенденции в лечении остеоартрита. Внутрисуставное применение производных гиалуроновой кислоты/ А. И. Найманн
Для цитирования: Лечащий врач № 7/2018; Номера страниц в выпуске: 42-45
Теги: суставы, воспаление, пожилые пациенты, боль




_575.gif)
.gif)