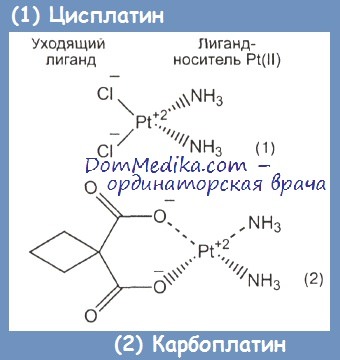
Что лучше карбоплатин или цисплатин
Противоопухолевой активностью обладает только цис-форма циспластина. Он действует как алкилирующий агент. Препарат проникает в клетку, где от молекулы отщепляется хлорид-ион, после чего цисплатин связывается с ДНК, образуя внутри- и межцепочечные сшивки. Препарат связывается главным образом с остатками гуанина. Назначается внутривенно.
Половина от введенного в организм количества препарата выводится через 40 мин; поздняя фаза выведения более продолжительна (период полувыведения составляет 60 ч). Порядка 90% лекарства связывается с белками плазмы, кроме того, оно проникает в почки, кишечник, печень, яичники и яички, но не попадает в ЦНС.
Цисплатин обладает высокой почечной токсичностью, и при назначении его в больших дозах крайне важно обеспечить повышенный отвод мочи. Для этого до введения препарата и в течение 24 ч после инъекции больному внутривенно вводят большое количество жидкости. При назначении дополнительных циклов терапии цисплатином может наблюдаться ухудшение функции почек. Поэтому следует регулярно проверять уровень креатинина в плазме и почечный клиренс.
Для поддержания отвода мочи на должном уровне при назначении больших доз препарата больным вводят маннит. Для предотвращения убыли из мочи ионов К+ и Mg2+/Ca2+ может потребоваться дополнительное одномоментное или длительное введение электролитов. При приеме препарата в больших дозах развивается сильная тошнота и рвота. Также отмечается необратимая ототоксичность, поэтому перед проведением курса лечения больному следует провести аудиометрию.
Миелопоэз подавляется лишь умеренно, однако часто развивается доклиническая форма периферической нейропатии. Нередко отмечается гиперчувствительность.
Цисплатин оказался высокоэффективным средством при лечении опухолей тестикулярного происхождения, и его комбинация с винбластином и блеомицином, на наш взгляд, оказала революционизирующее влияние на лечение больных с обширным опухолевым процессом. Препарат эффективен при лечении рака яичников, мочевого пузыря, а также лимфом и мелкоклеточной карциномы бронха. Противоопухолевый эффект цисплатина отмечен в случаях остеосаркомы и сквамозного рака головы и шеи.
Карбоплатин (Параплатин) для химиотерапии рака
Карбоплатин (Параплатин) аналог цисплатина отличается от него по характеру токсических проявлений, однако эффективен в отношении тех же типов опухолей. Препарат вводится внутривенно, причем площадь под кривой зависимости концентрации препарата от времени (AUC) описывается формулой AUC= [GFR (мл/мин) + 25 х n, где n представляет собой требуемое кратное число.
Препарат также проявляет меньшую токсичность по отношению к почкам и нервной системе. Карбоплатин назначают внутривенно в физрастворе или в смеси физраствора с глюкозой.
При отсутствии у больного рвоты, проведение процедур пре- и постгидратации не является необходимым. По сравнению с цисплатином, препарат менее эффективен при раке яичек. Это связано со снижением назначаемой дозы с целью предупредить опасность последствий подавления миелопоэза. Карбоплатин эффективен в лечении больных с мелкоклеточным раком легкого и пациенток с раком яичников. В последнем случае простота способа введения препарата делает его ценным для паллиативного лечения.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что лучше карбоплатин или цисплатин
Рак яичников – хроническое, фатальное, практически неизлечимое заболевание – большая проблема современной онкологии. Диагностика злокачественных новообразований яичников на ранних стадиях онкологического процесса затруднительна, в настоящий момент не существует специфических диагностических тестов, позволяющих выявить заболевание на начальных этапах развития.
Малосимптомное течение болезни, возможно, объясняется тем, что прогрессирование рака яичников происходит в основном путем диссеминации по париетальной и висцеральной брюшине. У 2/3 пациенток болезнь диагностируется на III–IV стадии заболевания, когда процесс распространяется за пределы малого таза, с вовлечением органов брюшной полости, отмечаются массивное поражение брюшины, асцит, опухолевый плеврит, гематогенные метастазы в печени, легких и костях [1]. Предлагаемые диагностические программы, включая лучевые способы диагностики и определения уровня онкомаркеров для выявления злокачественных новообразований яичников, не отвечают требованиям ВОЗ к скринингу в онкологии [2].
При эпителиальном раке яичников обладают противоопухолевой активностью около двух десятков химиопрепаратов. Однако лечение согласно существующим стандартам основывается на двух постулатах: основой терапии являются препараты платины, при этом цисплатин и карбоплатин в составе полихимиотерапии равноэффективны [3].
Цель исследования: оценить эффективность и безопасность химиопрепаратов, используемых в лечении первичного и рецидивирующего рака яичников. Проследить этапы эволюции современного стандарта лечения эпителиальных злокачественных новообразований яичников.
Как же формировался существующий на сегодняшний день «золотой стандарт» лечения рака яичников? Переворот в лечении рака яичников принадлежит цисплатину. Химиотерапия по схеме: цисплатин, доксорубицин и циклофосфан – стала стандартной с 1980-х гг., позволив увеличить продолжительность жизни больных с 14 до 24 месяцев (по сравнению с ранее применяемыми мелфаланом, тиофосфамидом, хлорамбуцилом) [4]. Платиновая полихимиотерапия в лечении распространенных форм рака яичников после оптимальных циторедуктивных операций позволила повысить 5-летнюю выживаемость лишь на 6% [5].
С 1992–1998 гг. начался следующий этап клинических исследований по изучению паклитаксела в терапии 1-й линии у пациенток с диссеминированным раком яичников. In vitro было установлено, что очень большое значение имеет последовательность введения химиопрепаратов: паклитаксел должен быть введен до производных платины [8]. Дело в том, что препараты платины увеличивают число клеток в S-фазе клеточного цикла, в то время как паклитаксел, действующий в G2/M фазе, оказывается неэффективным [9]. Кроме того, цисплатин, введенный перед паклитакселом, за счет уменьшения его плазменного клиренса значительно увеличивает токсичность последнего [6, 10]. В рандомизированном исследовании GOG-111 продемонстрировано значительное преимущество схемы ТР по сравнению с режимом СР: медиана выживаемости составила 38 месяцев по сравнению с 24 месяцами [11]. В исследовании OV-10 получены аналогичные результаты. В итоге режим ТР стал широко внедряться в повседневную клиническую практику онкологов.
В 1998–1999 гг. проанализирована возможность замещения цисплатина на карбоплатин ввиду нефро-, ото- и нейротоксичности цисплатина [6]. В то же время пути и способы введения цисплатина и таксанов в организм больных распространенным раком яичников имеют существенные различия. Наилучшие результаты по времени до прогрессирования заболевания оказались у больных с внутрибрюшинным введением цисплатина в сочетании с системной химиотерапией паклитакселом каждые 3 недели, до 6 курсов [4]. Стандарты лечения, даже «золотые», в 80% случаев не спасают больных распространенным раком яичников от рецидива заболевания, что настоятельно требует поисков дополнительных к химиотерапии способов воздействия на конкретные молекулярно-биологические механизмы в опухолевой клетке. В настоящее время мишенью для таргетного воздействия определен процесс ангиогенеза. Рандомизированные исследования по сравнению режимов «паклитаксел + цисплатин» и «паклитаксел + карбоплатин» продемонстрировали равную эффективность по непосредственным и отдаленным результатам на фоне гораздо более высокой токсичности комбинации с цисплатином.
При сравнении эффективности паклитаксела и доцетаксела (2004 г.) различий в выживаемости без прогрессирования, общей выживаемости, частоты объективных ответов не выявлено [6], при этом доцетаксел показал достоверно более высокую частоту нейтропении 3–4-й степени. Паклитаксел ассоциировался с более частым развитием нейропатии 2–4-й степени [6].
Ожидаемых результатов не дали исследования трехкомпонентных и последовательных режимов химиотерапии рака яичников, так же как и попытки улучшить результаты лечения за счет увеличения общего числа курсов [6].
Итак, комбинация карбоплатина в дозе (AUC 5–7) и паклитаксела в дозе 175 мг/м 2 один раз в три недели общим количеством 6 (8) циклов была признана «золотым стандартом» первой линии химиотерапии эпителиального рака яичников [6].
Платформой для интеграции бевацизумаба в режимы лечения рака яичников стали исследования III фазы GOG 218 (2010 г.), которые сравнивали три варианта лечения: стандартная ХТ (паклитаксел + карбоплатин), стандартная ХТ + бевацизумаб на протяжении 6 курсов ПХТ, стандартная ХТ с бевацизумабом на протяжении 15 месяцев либо до прогрессирования заболевания. Медиана выживаемости без прогрессирования процесса составила 10,3 месяца, 11,2 месяца, 14,1 месяца соответственно, однако это не влияло на общую выживаемость больных [12].
По результатам анализа ICON 7 было показано, что при подключении бевацизумаба на фоне химиотерапии и потом в качестве поддерживающей терапии в течение года можно увеличить медиану продолжительности жизни на 9,5 месяцев у нерезектабельных больных, а также больных с III–IV стадиями после неоптимальных циторедуктивных операций [13].
Безопасность добавления бевацизумаба к еженедельным введениям паклитаксела оценили в представленном на ASCO 2012 г. однорукавном исследовании OCTAVIA. Наиболее частыми нежелательными явлениями III–IV степени была нейтропения (60%), анемия (8%), тромбоцитопения (7%).
Побочные эффекты бевацизумаба связаны с прямым нарушением взаимодействия рецептора и лиганда сосудистого эндотелиального фактора роста (VEGFR/VEGF). Так, артериальная гипертензия отмечена в 4,2%, тромбозы – в 6,3%, кровотечения из слизистых и опухоли, так же как и перфорация желудочно-кишечного тракта, – в 0,5% случаев. Примечателен тот факт, что, несмотря на низкий уровень перфорации на фоне лечения (не более 4% по данным разных исследователей), этот показатель за счет развивающихся осложнений может увеличить общую летальность больных до 21,7%, снижая общий эффект от применяемого лечения. Продолжительность гипертензии определяется временем подавления VEGF, а влияние бевацизумаба на уровень артериального давления является дозозависимым. Сочетание ингибитора VEGF и химиотерапии (проанализированы результаты у 1745 пациенток) приводит к двукратному увеличению риска тромбозов по сравнению только с химиотерапией без включения бевацизумаба. Показанием для отмены таргетных препаратов являются клинические проявления тромбоза [14]. Помимо этого, в преклинических исследованиях показано дозозависимое нарушение заживления ран на фоне терапии бевацизумабом за счет нарушения неоваскуляризации и развития гипоксии. В связи с этим бевацизумаб не рекомендован в качестве неоадъювантного препарата в лечении рака яичников.
Прежде чем говорить о химиотерапии, применяемой при лечении рецидивов рака яичников, необходимо сказать, что данное заболевание, в отличие от других солидных опухолей, имеет ряд особенностей: исходное выявление распространенных стадий в 2/3 случаев; высокую чувствительность к цитостатикам; чрезвычайную склонность к возникновению рецидивов (практически 100%). В связи с этим не так важно, какая по счету линия химиотерапии назначена больной. Более существенным будет разделить рецидивы рака яичников на 2 подгруппы: платиночувствительные и платинорезистентные рецидивы. Такая градация обусловлена временем возникновения рецидива и, как следствие, потенциальным ответом на препараты платины. Как известно, платинорезистентным называется рецидив, зарегистрированный в течение первых шести месяцев после завершения первой линии химиотерапии. Наиболее неблагодарными и тяжелыми в лечении являются так называемые платинорефрактерные рецидивы, когда на фоне терапии первой линии наступает возврат болезни. Благоприятными в прогностическом отношении считаются платиночувствительные рецидивы, где интервал между окончанием предыдущей линии химиотерапии и возвратом заболевания составляет 6 месяцев и более.
Тем не менее лечение любого рецидива является паллиативным и направлено на устранение симптомов заболевания и улучшение качества жизни больных. Положительно зарекомендовали себя следующие схемы, используемые для лечения платиночувствительных рецидивов: гемцитабин + карбоплатин (отличается высокой гематологической токсичностью, в связи с чем далеко не всегда удается ввести гемцитабин в 15-й день), карбоплатин + пегилированный липосомальный доксорубицин (на первый план выходит кожная токсичность – ладонно-подошвенный синдром), цисплатин + пероральный этопозид (лейкопения, тромбоцитопения). Во всех исследованиях показано достоверно значимое увеличение времени до прогрессирования заболевания на фоне отсутствия достоверных различий в общей продолжительности жизни [4, 15]. Выбор схемы лечения во второй линии зависит от переносимости, удобства введения и токсичности цитостатиков, и, как ни банально это звучит, наличия лекарственного препарата в лечебном учреждении. Если интервал между завершением первой линии химиотерапии и возникновением рецидива составил более 1 года, можно вернуться к схеме карбоплатин – паклитаксел (исследование AGO-OVAR).
При платинорезистентных интервалах ожидаемая продолжительность жизни (при учете назначения второй линии химиотерапии) в среднем менее года. Применяют паклитаксел в монорежиме и в комбинации с эпирубицином, топотеканом, трабектидином, пегилированным липосомальным доксорубицином [4]. Важно отметить, что комбинированная терапия в этих случаях не приводит к улучшению отдаленных результатов, при этом значимо увеличивается выраженность токсических реакций. Большинство из перечисленных цитостатиков имеют примерно одинаковую эффективность. В результате стандартом лечения платинорезистентного рака является монохимиотерапия неплатиновым агентом. В исследовании AURELIA показано, что добавление бевацизумаба к монотерапии паклитакселом (еженедельное введение), топотеканом или пегилированным липосомальным доксорубицином значимо увеличивает медиану времени до прогрессирования от 3,4 месяца до 6,7 месяца [16]. Анализируя полученные данные, исследователи пришли к выводу, что бевацизумаб – эффективный препарат как при рецидивах заболевания, так и в первой линии лечения [17, 18]. При лечении рецидивов заболевания бевацизумаб достоверно увеличивает как выживаемость без прогрессирования, так и общую выживаемость больных [19]. В первой линии лечения бевацизумаб увеличивает выживаемость без прогрессирования, не оказывая существенного влияния на общую выживаемость.
Согласно клиническим рекомендациям от 2018 г. применение бевацизумаба рекомендовано при лечении первичного рака яичников, а также при рецидивах в дозе 7,5 или 15 мг/кг с интервалом в три недели, в течение 18–22 курсов (или до прогрессирования, но только в том случае, если оно не наступит раньше), начиная с 1-го или 2-го курса химиотерапии [20].
При рецидивах после окончания второй или третьей линии химиотерапии применять бевацизумаб следует до прогрессирования заболевания или возникновения неприемлемой токсичности.
Из перспективных агентов направленного действия необходимо отметить уже включенный в рекомендации олапариб (PARP-ингибитор). Этот препарат наиболее эффективен у больных с наследственными мутациями генов BRCA1/2. По данным исследований III фазы SOLO2/ENGOT-Ov21 поддерживающая терапия олапарибом достоверно (более чем в 3 раза) увеличила время без прогрессирования [21]. Важно отметить удобство применения препарата – пероральная форма и амбулаторное применение позволяют пациентке вести обычный образ жизни без ограничений, накладываемых регулярными госпитализациями. Наиболее частыми нежелательными явлениями являются анемия, астения или усталость, нейтропения 3-й и 4-й степени. У 2% больных зарегистрирована кишечная непроходимость. Олапариб одобрен для клинического применения и рекомендован при серозной аденокарциноме высокой степени злокачественности, наличии герминальной или соматической мутации BRCA, при платиночувствительных рецидивах [22].
Заключение. Подводя итог, можно сделать вывод, что поиски и разработки эффективных схем лечения как первичного, так и рецидивирующего рака яичников остаются актуальными и требуют дальнейшего изучения. Успехи в достижении большего времени без прогрессирования заболевания с применением таргетных препаратов нивелируются отсутствием увеличения общей продолжительности жизни больных и частотой и выраженностью побочных эффектов. Согласно клиническим рекомендациям в случае неэффективности двух режимов химиотерапии дальнейшее проведение химиотерапии сомнительно ввиду прогнозируемой низкой эффективности. В данном случае рекомендованы либо симптоматическая терапия, либо включение в клинические исследования.
Вспоминая слова одного из основателей отечественной терапевтической школы Матвея Яковлевича Мудрова: «Не стоит лечить болезни по одному только ее имени, а должно лечить самого больного, его состав, его организм, его силы», необходимо помнить о том, что стандарты не всегда работают, а в персонифицированном подходе к лечению в каждом конкретном случае есть будущее медицины.
Сравнение четырех схем химиотерапии для лечения распространенного немелкоклеточного рака легкого
Опубликовано в журнале: New England Journal of Medicine, 346: 92-98 (2002)
Дж.Г. Шиллер, Д. Харрингтон, Ч.П. Белам, К. Лангер, А. Сандлер, Дж. Крук, Дж. Жу и Д. Г. Джонсон от группы ECOG
Реферат
История вопроса.
Мы провели рандомизированное испытание в целью определить, будет ли какая-либо из трех схем химиотерапии превосходить комбинацию цисплатин/ паклитаксел у больных с распространенным немелкоклеточным раком легкого.
Методы.
1207 больных с распространенным немелкоклеточным раком легкого были рандомизированы на эталонную схему цисплатин/паклитаксел или на одну из трех экспериментальных схем: цисплатин/гемцитабин, цисплатин/доцетаксел или карбоплатин/паклитаксел.
Результаты.
Процент ответа для 11 больных, удовлетворяющих критериям испытания, составлял 19%, медианная выживаемость равнялась 7,9 месяца (95%-ный доверительный интервал [ДИ] от 7,3 до 8,5), годичная выживаемость 33% (95%-ный ДИ от 30 до 36%) и двухгодичная выживаемость 11% (95%-ный ДИ от 8 до 12%).
Процент ответа и выживаемость не отличались достоверно для больных, назначенных на лечение цисплатином/паклитакселом, и больных, назначенных на любую из трех экспериментальных схем. Лечение цисплатином и гемцитабином давало достоверно большее время до прогрессии заболевания по сравнению с лечением цисплатином и паклитакселом, однако давало большую вероятность почечной токсичности степени 3, 4 и 5 (у 9% больных по сравнению с 3% больных, получавших схему цисплатин/паклитаксел). Для больных с функциональным статусом 2 процент выживания был достоверно меньшии по сравнению с больными с функциональным статус 0 или 1.
Выводы.
Ни одна из четырех схем химиотерапии не давала достоверного преимущества по отношению к другим при лечении распространенного немелкоклеточного рака легкого.
Приблизительно треть всей онкологической смертности обусловлена раком легкого, который отвечает за большее количество летальных исходов каждый год, чем рак молочной железы, простаты и толстой кишки совместно. Медианная выживаемость для больных с нелеченым метастатическим немелкоклеточным раком легкого составляет всего лишь 4-5 месяцев, а процент выживания за 1 год всего лишь 10% [1].
Химиотерапия распространенного немелкоклеточного рака легкого часто считается неэффективной или слишком токсичной. Однако мета-анализы показали, что по сравнению с поддерживающим уходом химиотерапия дает небольшое преимущество по выживаемости у больных с немелкоклеточным раком легкого 2, Кроме того, рандомизированные испытания по сравнению химиотерапии с «наилучшим поддерживающим уходом» показали, что химиотерапия снижает симптоматику и улучшает качество жизни [5].
На протяжении последнего десятилетия появился ряд новых препаратов для лечения метастатического немелкоклеточного рака легкого, включая таксаны, гемцитабин и винорелбин. Комбинация одного или нескольких таких препаратов с препаратом платины дает более высокие проценты ответы и увеличивает выживаемость за 1 год, по данным исследований по фазе II [(6-10]. Однако, сравнения между этими более новыми схемами химиотерапии, которые часто используются в настоящее время, немногочисленны.
ECOG провела рандомизированное клиническое испытание по сравнению эффективности трех обычно используемых схем со стандартной схемой цисплатин/паклитаксел [11]. Главная цель испытания заключалась в том, чтобы сравнить общую выживаемость у больных, получающих лечение двойными комбинациями цисплатином/гемцитабином, цисплатином/доцетакселом, карбоплатином/паклитакселом и цисплатином/паклитакселом.
МЕТОДЫ
Больных с немелкоклеточным раком легкого на стадии IIIB (со злокачественным выпотом в плевру или перикард), стадии IV или с рецидивом заболевания рандомизировали в одну из четырех групп лечения (Рис. 1). Первая группа получала стандартное лечение: 135 мг/м 2 паклитаксела вводили на протяжении 24 часов в первый день с последующим введением цисплатина в дозе 75 мг/м 2 в день 2. Курс повторяли один раз в 3 недели. Во второй группе гемцитабин в дозе 1000 мг/м 2 вводили в дни 1, 8 и 15, а цисплатин в дозе 100 мг/м 2 вводили в первый день 4-недельного курса.
Больные в третьей группе получали доцетаксел в дозе 75 мг/м 2 и цисплатин в дозе 75 мг/м 2 в день 1, курс повторяли один раз в 3 недели. Больные в четвертой группе получали паклитаксел в дозе 225 мг/м 2 путем 3-часового вливания в день 1 с последующим вливанием карбоплатина в тот же день в дозе, рассчитанной для создания AUC равной 6. Курс повторяли раз в 3 недели. Больных стратифицировали в соответствии с функциональным статусом по ECOG (0-1 или 2, где больший балл говорит о больших нарушениях), потерей веса за предыдущие 6 месяцев ( 3 и тромбоцитов не менее 100000/мм 3 ); адекватную функцию печени (по критерию уровня билирубина не более 1,5 мг на децилитр, [или 25,6 мкмоля/литр]) и достаточную функцию почек (уровень креатинина не более 1,5 мг/децилитр, [или 132,6 мкмол/л]). Предшествующая лучевая терапия симптоматических очагов допускалась при условии, что индикаторные очаги (очаги, за которыми наблюдали, чтобы определить наличие ответа на лечение) не были облучены и что лучевая терапия была завершена до начала химиотерапии. Больные со стабильными метастазами в мозг могли участвовать в испытании. Все больные после информирования должны были предоставить согласие на участие.
Использовались стандартные критерии определения ответа [по ECOG]. Полный ответ определялся как отсутствие заболевания во всех известных локализациях, по крайней мере, в течение 4 недель. Частичный ответ определялся как 50%-ное снижение суммы произведений взаимно-перпендикулярных диаметров всех измеримых очагов, продолжавшееся, по крайней мере, 4 недель. Прогрессирующее заболевание определялось или как 25%-ное увеличение площади любого очага по сравнению с предыдущим измерением, или появление одного или нескольких новых очагов.
Выживание рассчитывали с даты записи в испытание до даты смерти или даты, когда о больном было последний раз известно, что он жив. Время до прогрессии заболевания рассчитывали, начиная с даты включения в испытание до даты регистрации прогрессии заболевания или смерти; данные о больных, которые были живы и не имели рецидива, снимались с учета (цензурировались) на дату последнего обследования.
Протокол был утвержден соответствующей комиссией по рассмотрению в каждом из участвовавших центров. Все больные после информирования представили письменное согласие на участие.
Статистический анализ
Основным учетным критерием было время выживания с момента включения в испытание. Первичный анализ, определенный протоколом, включал сравнение каждого из распределений по выживаемости для трех экспериментальных групп лечения с распределением для соответствующей контрольной эталонной группы с использованием двустороннего лог-рангового критерия [12]. Для контроля ошибки типа I (то есть для контроля на множественные сравнения) для каждого из сравнений использовалось номинальное двустороннее значение Р=0,016. Исследование было спланировано таким образом, чтобы дать 80%-ную возможность выявления увеличения медианной выживаемости в экспериментальных группах на 33%, то есть медианного выживания, составляющего 12 месяцев, поскольку по данным предыдущего испытания стандартная схема давала медианную выживаемость, равную 9 месяцам [11]. Полное разрешающая сила для выявления 33%-ного улучшения выживаемости потребовала бы всего приблизительно 1070 летальных исходов в четырех группах или 535 на одно попарное сравнение. На основании данных по включению больных и критерию участия для предыдущих испытаний ECOG мысчитали, что нам необходимо включить по 300 больных в каждую группу лечения на протяжении 30-месячного периода.
Промежуточные анализы в ходе испытания мониторировались комитетом по мониторингу данных ECOG. План испытания предполагал два промежуточных анализа и один окончательный анализ данных по выживаемости с использованием границы О’Брайена-Флеминга [13], когда имеется 33%, 67% и 100% ожидаемого количества летальных исходов.
Все приведенные значения Р являются двусторонними и были скорректированы на промежуточные анализы в соответствии с методом О’Брайена-Флеминга. Все распределения времени до события были оценены по методу Каплана-Мейера [14]. Все описанные сравнения в отношении сроков до наступления события проводились с использованием лог-рангового критерия. Категорийные данные, такие как данные о лечении, ответе и токсических эффектах, сравнивались для разных групп лечения с использованием точного критерия Фишера (15).
РЕЗУЛЬТАТЫ
В период с октября 1996 г. по май 1999 г. в испытание было включено всего 1207 больных. Медианный период наблюдения составлял 8,0 месяца. На 1 мая 2000 г.
умерло 1074 больных. Из 1207 больных, включенных в испытание, 52 (4,3%), как было обнаружено в последующем, не удовлетворяли критериям участия (Таблица 1).
Таблица 1. Характеристики больных
Характеристика
Цисплатин/ паклитаксел
(N=303)
Цисплатин/ гемцитабин
(N=301)
Цисплатин/ доцетаксел
(N=304)