Химиотерапия рака мозга
При химиотерапии лекарственные препараты применяются для уничтожения или повреждения раковых клеток. поскольку большинство препаратов с трудом проникают через гематоэнцефалический барьер, защищающий головной мозг, химиотерапия не является эффективным методом лечения при низкой степени злокачественности. На химиотерапию реагируют не все опухоли. Химиотерапия при опухолях головного мозга назначается после операции или лучевого лечения.
От способа введения лекарственного препарата зависит его вид. «Системные» препараты, которые проникают в головной мозг с кровью, могут вводиться перорально (внутрь через рот), внутривенно, внутримышечно или внутриартериально. «Местные» препараты вводятся внутрь опухоли или вокруг опухоли мозга.
Новые методы введения препаратов:
Химиотерапевтические препараты и схемы химиотерапии
При химиотерапии используются различные лекарственные препараты и их сочетания. К стандартным препаратам относятся:
Темозоломид (Темодал).
Темозоломид одобрен для лечения взрослых пациентов с анапластической астроцитомой, которая не реагирует на другое лечение. Кроме этого, он используется во время и после лучевой терапии по поводу впервые выявленной мультиформной глиобластомы. Для пациентов с глиобластомой в настоящее время терапией первой линии является сочетание радиотерапии и темозоломида с последующим ежемесячным введением данного препарата после завершения лучевого лечения. У пациентов с некоторыми генетическими особенностями препарат работает эффективнее. Побочные эффекты темозоломида относительно легкие, однако могут возникать запоры, тошнота и рвота, слабость и головная боль. Препарат принимается в виде таблеток.
Кармустин.
Для лечения многих видов опухолей мозга, включая глиобластому, медуллобластому и астроцитому применяется кармустин. Обычно препарат вводится внутривенно. Также он может использоваться в виде капсул-имплантатов (Глиадель), которые помещаются в полость, образующуюся после хирургического удаления опухоли. При внутривенном введении кармустина могут возникать такие побочные эффекты, как тошнота и рвота, слабость, дыхательные осложнения и появление в легких рубцовой ткани (легочный фиброз). Внутривенное введение кармустина может вызывать нарушение работы костного мозга, что приводит к уменьшению образования эритроцитов (так называемая миелосупрессия). При введении кармустина с помощью капсул могут возникать судороги, отек вещества головного мозга и инфицирование ткани мозга.
Другие химиотерапевтические препараты.
Исследователи изучают вопрос, могут ли препараты, которые используются для лечения других видов рака, помочь при опухолях головного мозга. К таким препаратам относятся:
Другим противоопухолевым препаратом является иринотекан (Кэмпас), применение которого изучается в составе комбинированного лечения.
Биологические лекарственные препараты (прицельная терапия)
Эффективными являются общепринятые химиотерапевтические препараты. Но они не делают различий между опухолевыми и здоровыми клетками. Они обладают общей токсичностью и вызывают ряд тяжелых побочных эффектов. «Направленные» биологические препараты действуют на молекулярном уровне, блокируя специфические механизмы, которые связаны исключительно с ростом и делением клеток опухоли. Побочные эффекты биологических препаратов не так ярко выражены, так как они прицельно действуют на раковые клетки. Использование данных препаратов дает возможность создания средств индивидуализированного лечения рака с учетом генотипа пациента.
Экспериментальные средства прицельной терапии.
В настоящее время в клинических исследованиях изучаются следующие средства прицельной терапии:
Что такое химиотерапия и как она проходит?
Оглавление
Химиотерапия является одной из основных методик лечения онкологических заболеваний. Проведение процедуры позволяет уничтожить раковые клетки и подавить их рост. Этот способ может повлечь за собой ряд побочных эффектов, поэтому каждая процедура должна проводиться исключительно под контролем опытных врачей и с соблюдением точных дозировок и схем. Обеспечить максимально возможную безопасность всех манипуляций могут только квалифицированные специалисты-онкологи.
Для чего проводится химиотерапия?
Лечение применяется для решения следующих основных задач:
Как основной метод химиотерапия назначается при системных злокачественных образованиях, поражающих весь организм (злокачественной лимфоме, лейкемии и др.). В остальных случаях такое лечение становится частью комплексного. Оно проводится вместе с операцией и облучением. Выполнять процедуры могут как после вмешательства, так и до него. Назначаются специальные препараты по разным схемам. Это позволяет увеличить их эффективность и сократить побочные эффекты отдельных средств.
Преимущества применения методики при онкологии
Суть химиотерапии заключается в том, что специальные препараты попадают в кровь и разносятся по всему организму, что позволяет системно воздействовать на него, уничтожая раковые клетки и метастазы вне зависимости от того, где они располагаются.
К основным достоинствам методики относят:
Виды химиотерапии
Назначается перед вмешательством с целью сокращения размеров новообразований. Такое лечение позволяет уменьшить риски возникновения метастазов.
Проводится после операции и предотвращает дальнейшее развитие опухоли, а также устраняет ее скрытые очаги. Данная терапия актуальна при любых видах рака и служит профилактической мерой.
Назначается при неоперабельных формах рака и доказала эффективность при повышенной восприимчивости клеток опухоли к противораковым препаратам.
Такую химиотерапию называют «горячей». Она предполагает воздействие на раковые клетки средств с высокими температурами. Методика особенно актуальна при опухолях больших размеров (в том числе в брюшине и костных тканях).
В рамках лечения применяются препараты с платиной. Используется методика при неэффективности иных средств терапии.
Проводится с использованием специальных составов, которые действуют на молекулярном уровне. Химиотерапия позволяет не просто остановить рост клеток и разрушить их, а запустить в них процессы самоуничтожения.
Выполняется с применением наименее агрессивных препаратов, отличающихся относительно небольшим количеством побочных воздействий. Лечение актуально при малых опухолях без метастазов.
Такая химиотерапия отличается высокими дозами используемых средств. Назначают ее преимущественно при устранении лимфом. К недостаткам методики относят высокую токсичность для организма пациента, большое количество негативных последствий и побочных эффектов.
Проводится на терминальной стадии болезни, когда обеспечивается поддержание жизнедеятельности организма, уменьшается дальнейший рост опухоли и облегчаются болевые ощущения.
Способы применения препаратов
Сегодня для выполнения химиотерапии применяется большое количество различных средств. Они выпускаются в виде таблеток и растворов для инъекций. Эффективность лечения во многом зависит именно от формы препаратов. Наилучших результатов можно достичь при внутривенном их введении. Такие средства быстро разносятся по всему организму с током крови, но при этом сокращают вред для органов желудочно-кишечного тракта. Препараты в таблетках могут использоваться даже в домашних условиях. Сегодня разработаны и средства местного действия. Они выпускаются в виде мазей и аппликаций. Используют их при лечении рака ротовой полости, кожи и др.
Важно! Внутривенно препараты могут вводиться посредством постановки уколов и капельниц.
Также по способу применения средства можно разделить на самостоятельные и применяемые в комплексе с другими методиками лечения: оперативными вмешательствами и лучевой терапией.
Важно! Так как многие из назначаемых составов являются токсичными и имеют большое количество побочных эффектов, на время терапии может потребоваться пребывание пациента в стационаре под контролем медицинского персонала. Если самочувствие больного является удовлетворительным, допустимо амбулаторное проведение процедур по введению препаратов.
Подготовка к химиотерапии
Перед началом лечения необходимо:
При необходимости обеспечивается и комплексная психологическая поддержка. Она позволяет настроиться на терапию, которая нередко является не просто достаточно сложной, но и длительной. Работу с пациентом осуществляют психологи и психотерапевты. Также важной является поддержка близких.
Как проводится терапия?
Лечение всегда выполняется по индивидуально подобранной схеме. Она зависит от целого ряда факторов, в числе которых:
Комплекс препаратов подбирается с учетом достижения максимального эффекта от каждого приема. При этом онкологи предлагают больным средства с минимально возможным количеством побочных реакций. Это позволяет сохранить здоровье и обеспечить нормальную жизнедеятельность организма.
Сколько длится терапия?
Продолжительность лечения всегда определяется индивидуально и во многом зависит от типа выявленной опухоли и ее чувствительности к тем или иным препаратам. Проводится оно циклами, которые длятся по 14 дней.
При этом введение средств может осуществляться:
Продолжительность одной процедуры обычно составляет 2-3 часа. Промежуток между сеансами определяется выбранной схемой химиотерапии. Общее количество циклов также варьируется и обычно составляет 4-8. Общая продолжительность лечения – от одного месяца до года. В некоторых случаях требуется повторная терапия с целью предотвращения рецидивов.
Противопоказания к химиотерапии
Лечение не проводится при:
Каждый курс начинается только после проведения необходимой диагностики и назначается исключительно онкологом. Только опытный врач может принять решение о том, возможно ли выполнение терапии в определенных условиях.
Побочные эффекты
После курса лечения зачастую отмечается выраженное ухудшение работы всего организма. Это связано со снижением количественных и качественных показателей крови и изменением ее состава. Также обостряются инфекционные заболевания, ухудшается общий иммунитет.
К последствиям химиотерапии относят:
Пациенты жалуются на быструю утомляемость, сонливость и слабость, депрессивный настрой. У некоторых людей отекают лицо, руки и ноги, немеют конечности, повышается кровоточивость слизистых оболочек. Нередко возникают и аллергические реакции, которые могут проявляться как небольшой сыпью, так и опасным отеком Квинке. Противоопухолевое лечение может спровоцировать болезненные ощущения во всем организме, чувство жжения, повышение температуры тела, ухудшение качества ногтей и др.
Анализы крови в процессе химиотерапии
Так как вводимые лекарственные препараты воздействуют не только на раковые, но и на здоровые клетки (в том числе крови), пациенты страдают от анемии и иных патологических состояний. Для контроля уровня показателей здоровья регулярно проводится лабораторная диагностика.
Больные сдают анализы крови. Как правило, отмечаются сниженные параметры лейкоцитов, тромбоцитов и эритроцитов. Врачи дают рекомендации по улучшению состояния здоровья. Назначаются специальные диеты, сокращаются нагрузки, в рацион обязательно вводятся витамины и микроэлементы.
Кроме того, пациентам советуют избегать переохлаждений, реже бывать в общественных местах, тщательно следить за личной гигиеной.
Сколько стоит химиотерапия?
Стоимость лечения зависит от целого ряда факторов и не может быть озвучена без их предварительной оценки.
Самой дорогой обычно является терапия опухолей мозга, крови и поджелудочной железы. Точную стоимость может рассчитать только специалист после оценки всех важных параметров предстоящих процедур.
Питание после лечения
Диета как во время, так и после химиотерапии должна быть калорийной и достаточно питательной. Рекомендовано употреблять большое количество белка, качественных жиров и углеводов.
Корректируется питание в зависимости от:
К основным разрешенным продуктам относят мясо птицы и кролика, свинину и говядину, сыр, свежие овощи, морскую рыбу, бобовые, цельнозерновой хлеб, сухофрукты и орехи, масла, пастилу и зефир. Отказаться следует от консервов и копченостей, алкоголя, жирных и жареных блюд, газированных напитков, чипсов и других снеков, сала, фаст-фуда.
Назначаемая диета всегда направлена на снижение побочных эффектов от проведенной химиотерапии и восстановление общих сил организма.
Важно! Следует понимать, что неполноценное питание может существенно ухудшить состояние больного. Тем не менее заставлять пациента есть нельзя, так как это может спровоцировать приступы тошноты и рвоты.
Преимущества проведения химиотерапии в МЕДСИ
Если вы планируете химиотерапию в МЕДСИ, обратитесь к нашим специалистам любым удобным способом и задайте им все возникшие вопросы.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ЛЕКАРСТВЕННОМУ ЛЕЧЕНИЮ ПЕРВИЧНЫХ ОПУХОЛЕЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ
Коллектив авторов: Кобяков Г. Л., Бекяшев А.Х., Голанов А.В., Коновалов А.Н., Насхлеташвили Д.Р., Потапов А.А., Рзаев Д.А., Рыжова М.В., Смолин А.В., Трунин Ю.Ю., Улитин А.Ю.
DOI: 10.18 027/2224–5057–2018–8–3s2–83–99
Ключевые слова: опухоли центральной нервной системы, коделеция 1p/19q, IDH-1 мутация, метилирование MGMT, первичная лимфома ЦНС, эпендимома, герминома ЦНС, медуллобластома
Цитирование: Кобяков Г. Л., Бекяшев А. Х., Голанов А. В., Коновалов А. Н., Насхлеташвили Д. Р., Потапов А. А. и соавт. Практические рекомендации по лекарственному лечению первичных опухолей центральной нервной системы // Злокачественные опухоли: Практические рекомендации RUSSCO #3s2, 2018 (том 8). С. 83–99
ISSN 2587-6813 (электронное издание)
Злокачественные опухоли. Том 8, #3, 2018, спецвыпуск 2
1. КЛАССИФИКАЦИЯ И ОПРЕДЕЛЕНИЕ СТАДИИ
TNM классификация в отношении первичных опухолей центральной нервной системы не применяется. Основным классификационным критерием, определяющим тактику лечения, является морфологическая классификация; рекомендуется использование классификации ВОЗ опухолей ЦНС 2016 г. (см. раздел 2.2. «Морфологический диагноз»).
2. ДИАГНОСТИКА
2.1. Обследование
сбор анамнеза, оценка неврологического и соматического статуса, а также функционального статуса по шкале Карновского;
МРТ головного и/или спинного мозга:
МРТ головного мозга в трёх проекциях в стандартных режимах (Т1, Т2, FLAIR, Т1 + контраст);
в случаях, когда МРТ не может быть выполнена (например, при наличии кардиостимуляторов или ферромагнитных имплантов), выполняется КТ с контрастным усилением и без него;
анализы: клинический, биохимический крови, общий анализ мочи, анализ свёртывающей системы крови, ВИЧ, гепатиты;
при показаниях (опухоль пинеальной области) — анализ крови на опухолевые маркёры АФП, β-ХГЧ, ЛДГ;
УЗИ вен нижних конечностей;
консультация офтальмолога (оценка глазодвигательных, зрительных нарушений, а также признаков внутричерепной гипертензии на глазном дне);
в процессе лечения регулярно должен проводиться контроль эффективности: МРТ с контрастным усилением и без него в трёх проекциях (или в одной проекции с режимом SPGR с последующей реконструкцией) и в стандартных режимах (Т1, Т2, FLAIR, Т1 + контраст). Частота выполнения зависит от гистологического диагноза и этапа лечения (см. Алгоритмы лечения). Оценка динамики опухоли проводится согласно критериям RANO.
функциональная МРТ двигательных и речевых зон; и МР-трактография; МР-ангиография, МР-спектроскопия, МР-перфузия;
при подозрении на опухоль с риском диссеминации по оболочкам головного и спинного мозга (медуллобластома, пинеобластома, первичные герминативно-клеточные опухоли ЦНС и пр.) выполняется МРТ всего спинного мозга с контрастным усилением;
ПЭТ/КТ головного мозга с аминокислотами (метионином, тирозином);
КТ головного мозга выполняется также в дополнение к МРТ в случаях костных опухолей, при показаниях — КТ-перфузия, КТ-ангиография;
консультация нейрохирурга (в специализированном нейрохирургическом центре или отделении), при необходимости — в федеральном нейрохирургическом центре;
консилиум с участием нейрохирурга, рентгенолога, радиолога, онколога.
2.2. Морфологический диагноз
Во всех случаях следует стремиться к гистологической верификации опухоли; диагноз формулируется в соответствии с классификацией ВОЗ опухолей ЦНС 2016 г. В дополнение к основному диагнозу указывается степень злокачественности опухоли G (от I до IV ст.).
У пациентов с глиальными опухолями определяются также мутация генов IDH‑1,2, метилирование гена MGMT, коделеция 1p/19q. При отсутствии технической возможности определения данных мутаций, используется аббревиатура «NOS».
Морфологическая верификация может не проводиться, если получение диагностического материала сопряжено с высоким риском осложнений, например, при диффузных опухолях ствола головного мозга.
3. ЛЕЧЕНИЕ
Стандартными методами лечения первичных опухолей ЦНС являются хирургический, лучевой и лекарственный.
3.1. Хирургическое лечение
Хирургическое удаление производится для максимально возможного уменьшения объёма опухоли с целью разрешения внутричерепной гипертензии, уменьшения неврологического дефицита и получения достаточного количества морфологического материала. В послеоперационном периоде после удаления опухоли обязательно выполнение КТ с контрастированием и без него, а также выполнение МРТ с контрастным усилением и без него в течение 24–72 часов.
СТБ или навигационная биопсия должны быть использованы в случаях, когда хирургическое удаление невозможно или нецелесообразно, а также при подозрении на первичную лимфому ЦНС.
В исключительных случаях, например, у пациентов пожилого возраста, пациентов с грубой неврологической симптоматикой, при расположении опухоли в жизненно важных структурах (в том числе в стволе мозга) ХТ и/или ЛТ могут применяться на основании данных нейровизуализации и клинической картины по решению консилиума.
3.2. Лучевая терапия
Дистанционные методы ЛТ являются основным компонентом лечения большинства пациентов с опухолями ЦНС.
Лучевое лечение используется у первичных больных после хирургического удаления/биопсии опухоли, а также при возникновении рецидива/продолженного роста опухоли. ЛТ может проводиться как на область опухоли (на остаточную опухоль или на ложе опухоли), так и на пути возможного метастазирования (например — краниоспинальное облучение в лечении эпендимомы). Золотым стандартом лучевого лечения является применение стереотаксической техники облучения.
3.2.1. Режимы фракционирования
Режим стандартного фракционирования: 1 сеанс в день РОД 1,8–2,2 Гр до СОД 24–70 Гр; используется у пациентов с крупными и/или диффузно-растущими опухолям и различной гистологической природы (в основном — глиомы G I–IV), а также при облучении путей возможного метастазирования опухоли (краниоспинальное облучение).
Радиохирургическое лечение — одномоментное подведение высокой дозы (12 Гр и более) с использованием стереотаксической техники. Используется у пациентов с небольшими опухолями (до 3 см в максимальном измерении), имеющими чёткие границы (пилоидные астроцитомы, эпендимомы, менингиомы, невриномы, аденомы гипофиза, краниофарингиомы и пр.).
Режим гипофрационирования (РОД ≥ 2,5 Гр, СОД ≥ 15 Гр) используется у пациентов с опухолями, имеющими чёткие границы, либо с минимальной зоной возможной инфильтрации тканей (до 3–5 мм), а также у пациентов с образованиями более 3 см и/или с опухолями, располагающимися вблизи критических структур мозга.
При лечении злокачественных опухолей (G III–IV) ЛТ следует начинать в сроки от 2 до 6 нед. после операции, в ряде случаев в комбинации с ХТ (см. раздел «Химиотерапия»).
После ЛТ возможно возникновение постлучевых повреждений вещества головного мозга, в том числе лучевого некроза. Для дифференциации постлучевых осложнений и рецидива опухоли целесообразно использование дополнительного МРТ с контрастированием, ПЭТ головного мозга с метионином (тирозином), МР-спектроскопии, КТ-перфузии и др. В лечении лучевого некроза может использоваться бевацизумаб.
3.3. Лекарственная противоопухолевая терапия в комплексном лечении первичных опухолей ЦНС
Показания и выбор схемы противоопухолевой лекарственной терапии зависят от гистологического диагноза. Основные режимы ХТ первичных опухолей ЦНС приведены в табл. 1, 2, 3. В настоящем разделе представлены алгоритмы выбора тактики лечения в зависимости от нозологической группы.
3.3.1. Злокачественные глиомы
Подход к лечению зависит от степени злокачественности опухоли. Выделяют злокачественные (G III–IV) глиомы (анапластическая астроцитома, анапластическая олигодендроглиома, анапластическая олигоастроцитома, глиобластома, в том числе глиосаркома) и низкой степени злокачественности (G I–II), включающие в себя астроцитому, олигодендроглиому, олигоастроцитому, а также редкие типы опухолей — плеоморфную ксантоастроцитому, субэпендимарную гигантоклеточную астроцитому, пилоидную астроцитому.
МРТ признаками злокачественной глиомы являются гипоинтенсивная в Т1 режиме, гиперинтенсивная в режимах Т2 и FLAIR, сливающаяся с зоной перифокального отёка опухоль. Клинические признаки: короткий анамнез, быстрое нарастание симптомов, относительно редко наблюдается судорожный синдром. Если по данным МРТ нельзя исключить лимфому ЦНС, пациенту необходимо сначала выполнить СТБ.
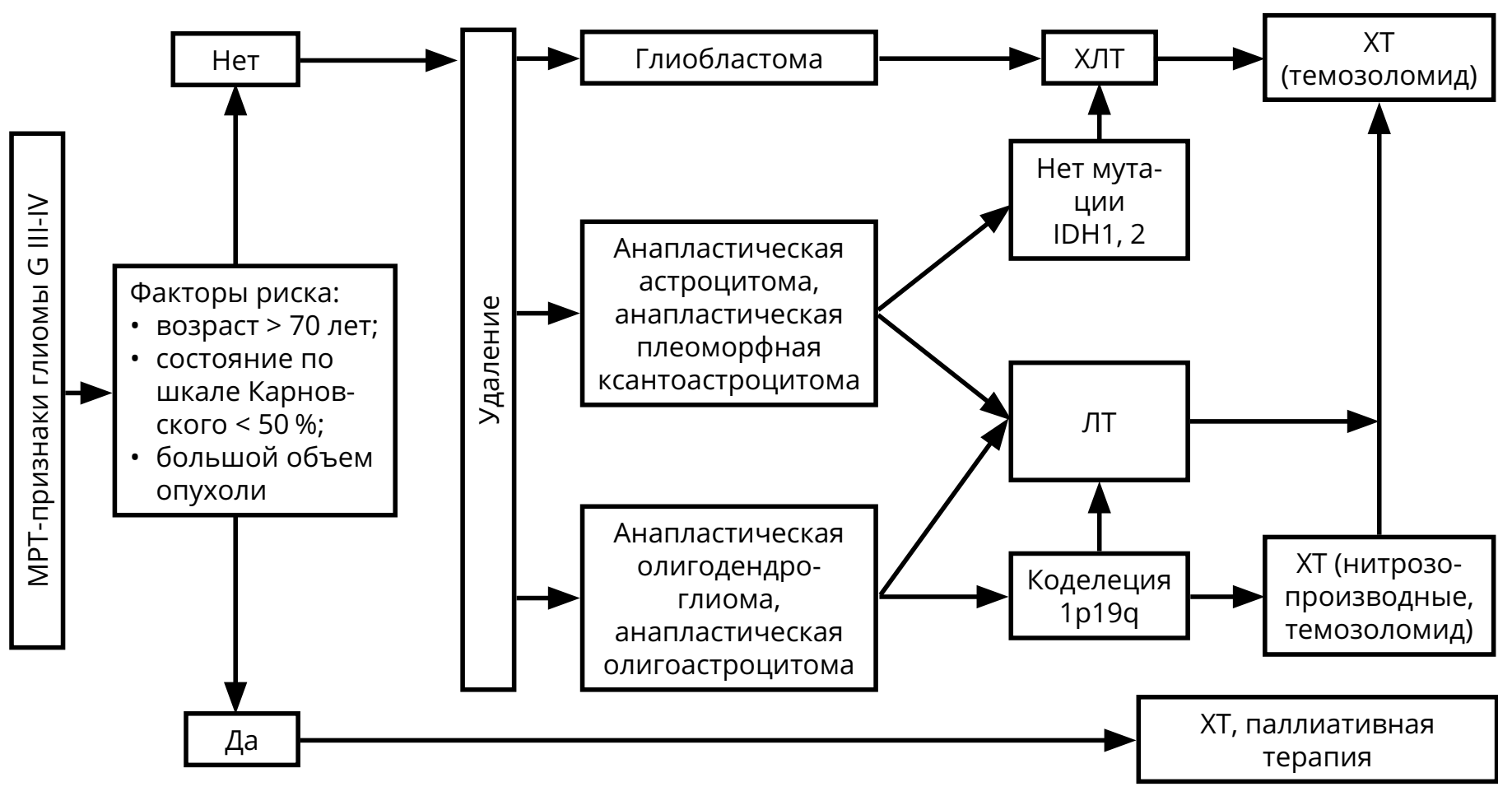
После хирургического вмешательства с верификацией диагноза астроцитарной глиомы G III–IV показано продолжение лечения в виде ЛТ и ХТ (рис. 1). Молекулярно-генетические факторы, определяющие прогноз — IDH-1,2 мутации, метилирование гена MGMT, коделеция 1p/19q (все — благоприятные).
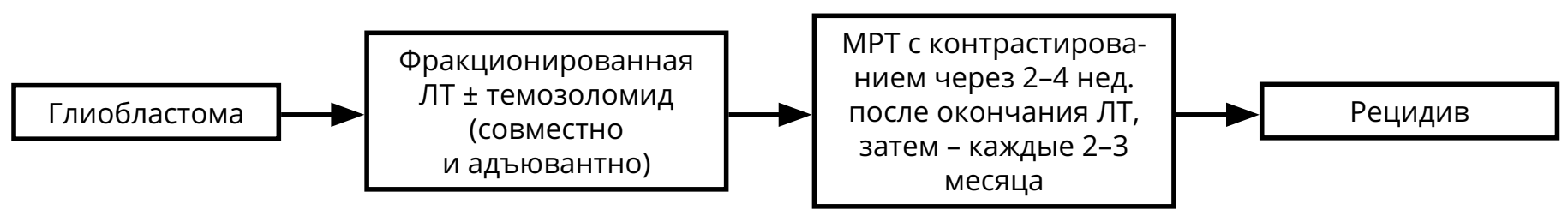
Для пациентов с глиобластомой режимом выбора послеоперационного лечения является ХЛТ с ежедневным приёмом темозоломида (75 мг/м 2 ) (в течение всего курса ЛТ — 30 фракций по 2 Гр на фракцию), с последующими 6–10 курсами темозоломида 5/23 (см. раздел 4).
Проведение ЛТ (30 фракций по 2 Гр на фракцию) показано для пациентов с анапластической астроцитомой, анапластической олигодендроглиомой, анапластической олигоастроцитомой.
При первом контроле после комбинированной ХЛТ глиомы (в течение 1 мес. после окончания ЛТ) можно наблюдать феномен псевдопрогрессии: увеличение контрастируемой части опухоли при отсутствии нарастания неврологических симптомов на фоне стабильных доз ГКС. В таком случае рекомендован МРТ-контроль через 1–3 мес. (то есть через 2–3 мес. после завершения ЛТ) с целью окончательной оценки динамики болезни.
ХТ (режим PCV или монотерапия ломустином или темозоломидом) должна быть назначена после ЛТ больным анапластической астроцитомой, анапластической олигодендроглиомой, анапластической олигоастроцитомой (см. раздел 4).
При коделеции 1p/19q у больных анапластической олигоастроцитомой и анапластической олигодендроглиомой в послеоперационном периоде могут быть назначены как ЛТ, так и ХТ (режим PCV или монотерапия темозоломидом 5/23). В случае полного ответа на химиотерапию ЛТ может быть отложена до рецидива заболевания.
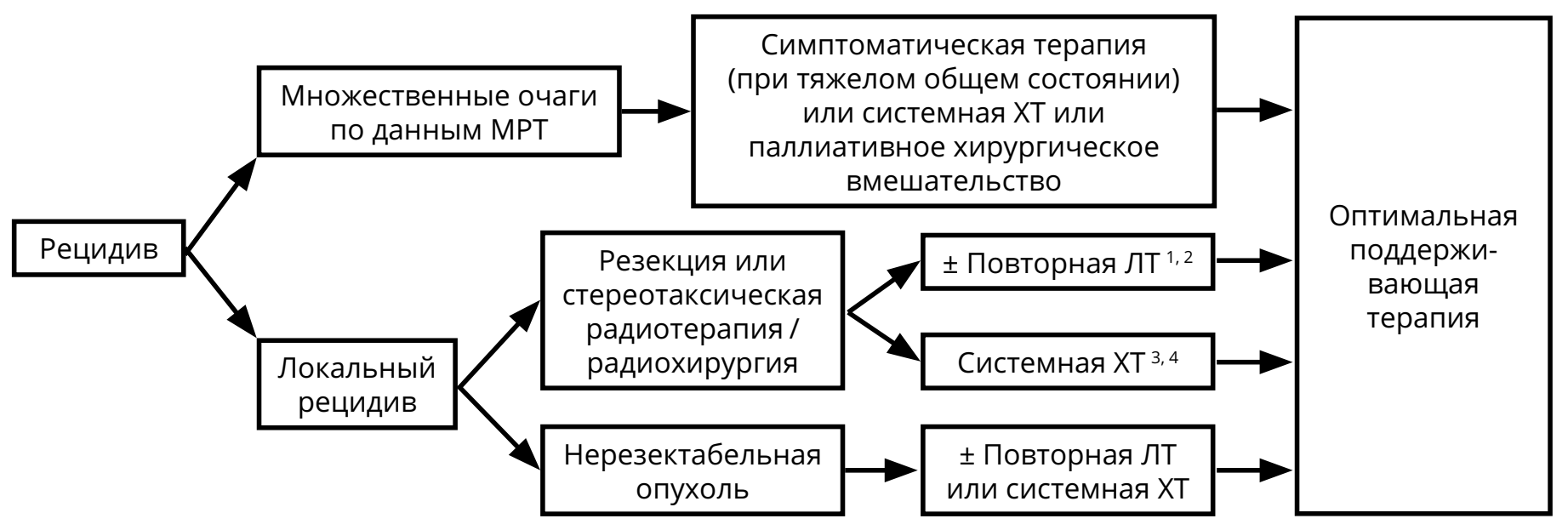
Методами лечения рецидивов глиом являются повторное хирургическое вмешательство, системная ХТ, повторная ЛТ и паллиативная терапия. Показания к назначению любого из этих методов лечения должны обсуждаться мультидисциплинарно. В некоторых случаях может быть предложена повторная ЛТ (если с момента предшествующей ЛТ прошло не менее 8 мес.). При небольших локальных рецидивах могут рассматриваться радиохирургические методики или гипофракционированная ЛТ.
2 Необходима МР-спектроскопия, МР-КТ перфузия, ПЭТ (с метионином) для исключения лучевого некроза, особенно, если интервал от первой ЛТ 18 мес.
3 При анапластической олигодендроглиоме и анапластической олигоастроцитоме предпочтительна ХТ.
4 Ответ после двух последовательных неэффективных режимов ХТ маловероятен.
В качестве ХТ рецидивов анапластических астроцитарных и олигодендроглиальных опухолей G III показано назначение темозоломида (если ранее не использовался или, если использовался, но был достаточно длительный — не менее 6 мес. — контроль болезни). Нитрозопроизводные могут также быть назначены, если они не использовались ранее. При олигодендроглиоме и анапластических олигоастроцитомах стратегия зависит от использованной ранее схемы лечения. В случае применения радиотерапии назначается ХТ PCV; если использовались радиотерапия и химиотерапия PCV, то предпочтение отдаётся ХТ темозоломидом. В случае первичной ХТ с использованием режима PCV, прежде всего, должна обсуждаться радиотерапия. Если радиотерапия не проводилась, то пациентам пожилого возраста, с обширным опухолевым поражением может быть предложена II линия ХТ (например, темозоломид после PCV).
3.3.2. Глиомы низкой степени злокачественности (G I–II)
3.3.2.1. Астроцитома, олигодендроглиома, олигоастроцитома G II
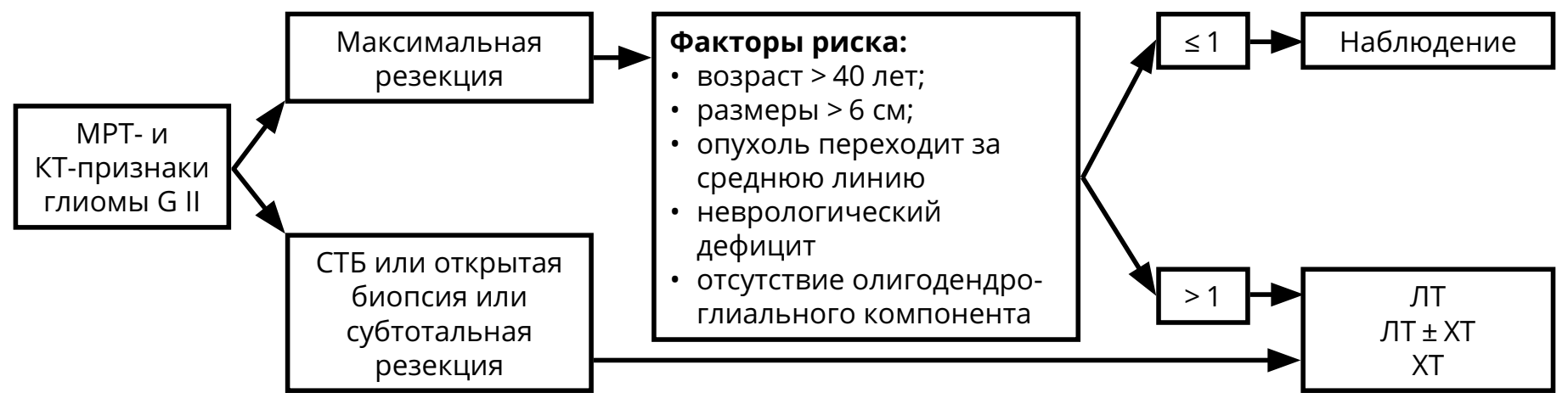
Предоперационный диагноз глиомы G II основан на МРТ-признаках (гиподенсивная в Т1 режиме, гиперденсивная в режимах Т2 и FLAIR, не накапливает контраст) и клинических проявлениях (длительный анамнез, часто — судорожный синдром, медленное нарастание симптомов). Для олигоденроглиомы и олигоастроцитомы характерно наличие кальцинатов на КТ. Послеоперационное лечение (ЛТ, ХТ) зависит от радикальности удаления и/или факторов риска (рис. 4). Коделеция 1p/19q и IDH-1,2‑мутации — прогностически благоприятные факторы.
В случае полной резекции опухоли и при наличии не более одного фактора риска показано наблюдение: МРТ 1 раз в 3–6 мес. или при нарастании симптомов (см. раздел 6 «Наблюдение»). При неполном удалении/биопсии опухоли или при наличии более одного фактора риска показано назначение ЛТ и/или ХТ.
Пациентам пожилого возраста (старше 70 лет) с обширными опухолями ЛТ может не проводиться (назначается монотерапия темозоломидом 5/23). Вопрос о назначение ЛТ и ХТ ослабленным пациентам (с низким индексом Карновского и/или с признаками внутричерепной гипертензии), большой распространённостью опухоли, решается индивидуально.
После окончания курса ЛТ должны быть назначены контрольные МРТ (через 2–4 нед. после окончания ЛТ, а затем каждые 2–3 месяца в течение 2–3 лет).
3.3.2.2. Плеоморфная ксантоастроцитома G II
Плеоморфная ксантоастроцитома на МРТ — как правило, кистозная, хорошо отграниченная от окружающего мозгового вещества опухоль, сóлидная часть которой интенсивно накапливает контраст и расположена асимметрично относительно кисты. Показано удаление опухоли. Адъювантная терапия не требуется. Следует указать, что в классификацию 2016 г. внесено понятие «анапластическая плеоморфная ксантоастроцитома G III». Лечение этой опухоли осуществляется по принципам лечения злокачественных глиом. Дополнительно определяется BRAF мутация (в случаях выявления может быть назначена терапия вемурафенибом или дабрафенибом).
3.3.2.3. Субэпендимарная гигантоклеточная астроцитома
Чаще всего является одним из проявлений туберозного склероза (болезни Бурневилля). На МРТ представлена солидной опухолью, расположенной чаще всего в проекции одного или обоих отверстий Монро, гиподенсивной в Т1‑режиме и интенсивно накапливающей контраст. На КТ характерно наличие симметричных кальцинатов в проекции зрительных бугров. Стандартом лечения этих опухолей является оптимальное (тотальное) удаление. Больным с диффузным поражением показано лечение эверолимусом.
3.3.2.4. Пилоидная астроцитома G I
Обычно встречается в детском возрасте и у молодых взрослых. Оптимальным методом лечения является хирургическое удаление (при условии операбельности опухоли). Обязательным является выполнение МРТ в послеоперационном периоде для оценки радикальности операции. В случае радикального удаления опухоли больному показано наблюдение. В случае остаточной опухоли показана ЛТ.
3.3.2.5. Глиоматоз головного мозга
Глиоматоз мозга — это диффузное поражение глиомой структур головного мозга (более 3‑х анатомических областей больших полушарий, обычно с переходом через мозолистое тело и с перивентрикулярным распространением). Показана верификация диагноза путём СТБ, так как от гистологического диагноза может зависеть выбор лечебной тактики (например, при олигодендроглиальных опухолях, как обычно, показано определение коделеции 1p/19q, при её выявлении — назначение ХТ на основе нитрозопроизводных). Могут рассматриваться три подхода: наблюдение (если у больного нет клинических симптомов заболевания), ХТ (PCV/ломустин/темозоломид) и ЛТ головного мозга в зависимости от клинической ситуации, данных нейровизуализации, морфологии, ИГХ и молекулярно-генетических маркёров и мнения специалистов.
3.3.2.6. Глиомы ствола головного мозга
При узловых формах опухолей ствола мозга, экзофитном характере роста, т.е. при МР-признаках полной или частичной отграниченности от структур ствола (например, при пилоидной астроцитоме) показано удаление опухоли (или открытая биопсия). Далее, в зависимости от гистологического диагноза, возраста и радикальности удаления назначаются ЛТ и/или ХТ. При диффузном характере роста опухолей ствола (например, при диффузной глиоме моста — «диффузной понтинной глиоме») показано использование ЛТ и ХТ без обязательной верификации. При ювенильных глиомах четверохолмной пластинки после разрешения гидроцефалии осуществляется регулярное клиническое и МРТ-наблюдение (в случае прогрессирования опухоли рассматривается вопрос об удалении с последующей ЛТ).
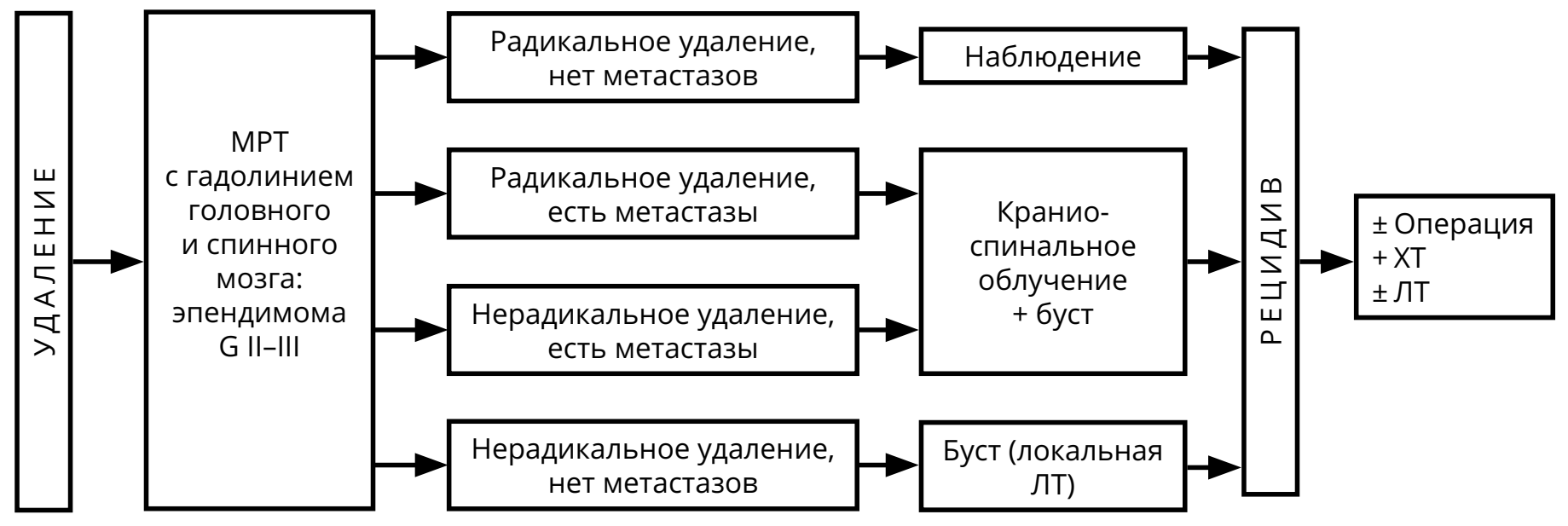
3.3.3. Эпендимомы
Редкие опухоли, возникающие из эпендимы головного мозга (чаще располагаются в пределах желудочковой системы, реже — экстравентрикулярно) или спинного мозга, примерно одинаково часто встречаются у детей и у взрослых. Приблизительно в половине случаев на КТ и МРТ выявляются признаки мелких кальцинатов. Хорошо накапливают контрастное вещество, чаще — негомогенно. По классификации ВОЗ 2016 г. выделяют эпендимому (G II) и анапластическую эпендимому (G III).
Ведущую роль в лечении эпендимомы играет хирургическое удаление опухоли. Поэтому при выполнении операции следует стремиться к максимальной резекции опухоли. При установлении гистологического диагноза эпендимомы или анапластической эпендимомы показано проведение МРТ головного и спинного мозга с контрастированием (с целью определения радикальности операции и выявления возможных спинальных метастазов) и исследование спинномозговой жидкости на опухолевые клетки.
В случае выполнения максимальной резекции эпендимомы рекомендовано наблюдение (при отсутствии признаков метастазирования в виде наличия клеток опухоли в ликворе или спинальных метастазов на МРТ спинного мозга с контрастом). При невозможности радикальной операции или наличии резидуальной опухоли после хирургического вмешательства, адъювантным методом лечения является ЛТ, объём которой определяется радикальностью операции и выявленной распространённостью опухоли (рис. 5). ХТ может использоваться в случаях рецидива эпендимомы (рис. 6). Режимы ХТ при эпендимомах указаны в разделе 4.
1 Объём ЛТ зависит от объёма предшествующей ЛТ, распространённости опухоли и времени, прошедшего с момента предшествовашей ЛТ.
Контрольные обследования (МРТ с контрастированием и клиническое обследование) осуществляются не реже 1 раза в 3 мес. на протяжении первого года наблюдения, затем при отсутствии данных за прогрессирование — не реже 1 раза в 6 мес. В случае прогрессирования в виде солитарного очага рассматривается вопрос о повторной операции или, при небольших размерах рецидива, о радиохирургическом лечении.
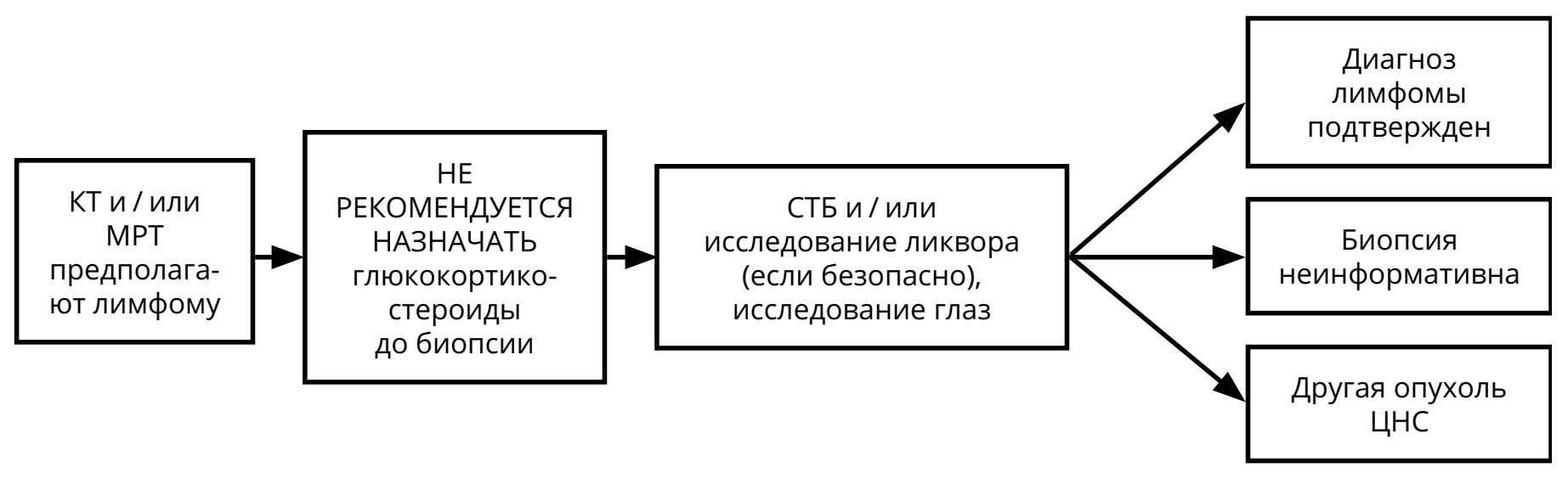
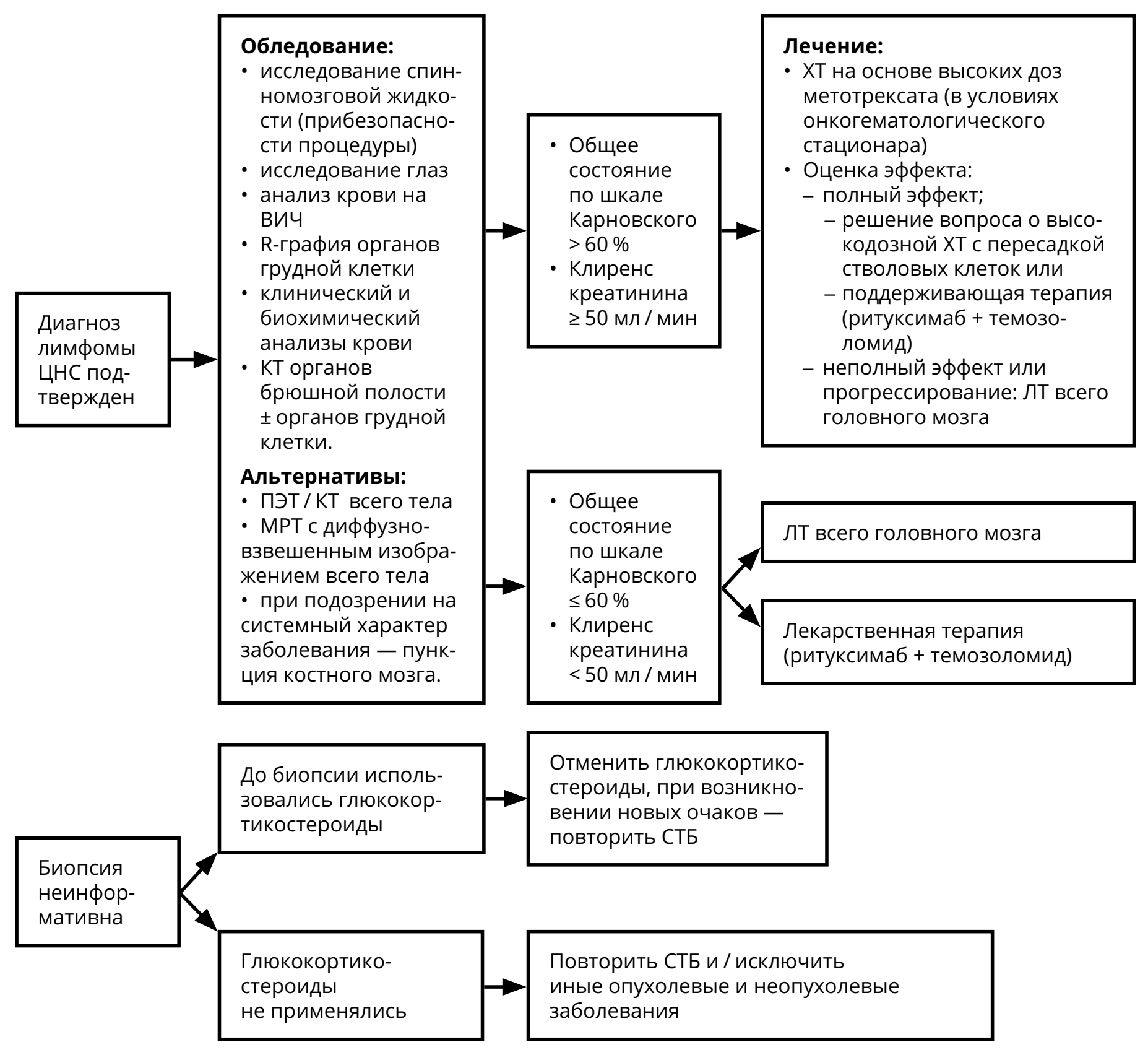
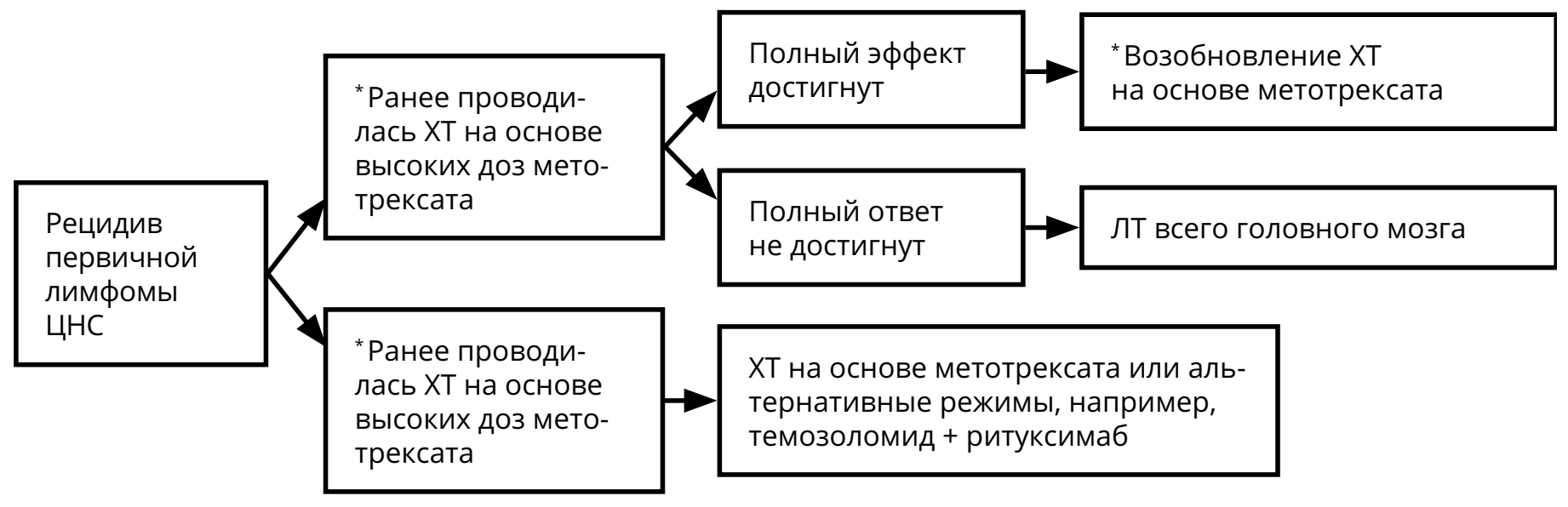
3.3.4. Первичная лимфома ЦНС
Относительно редкая опухоль ЦНС (5–7 % от всех первичных опухолей ЦНС), относящаяся, согласно онкогематологическим классификациям, к редким формам неходжкинских экстранодальных лимфом. Морфологически более, чем в 90 % случаев представлена диффузной B-клеточной лимфомой. Различают лимфомы ЦНС у иммунокомпетентных пациентов и ВИЧ-ассоциированные лимфомы. У 15–20 % больных с первичными лимфомами ЦНС выявляется поражение опухолью стекловидного тела глаза.
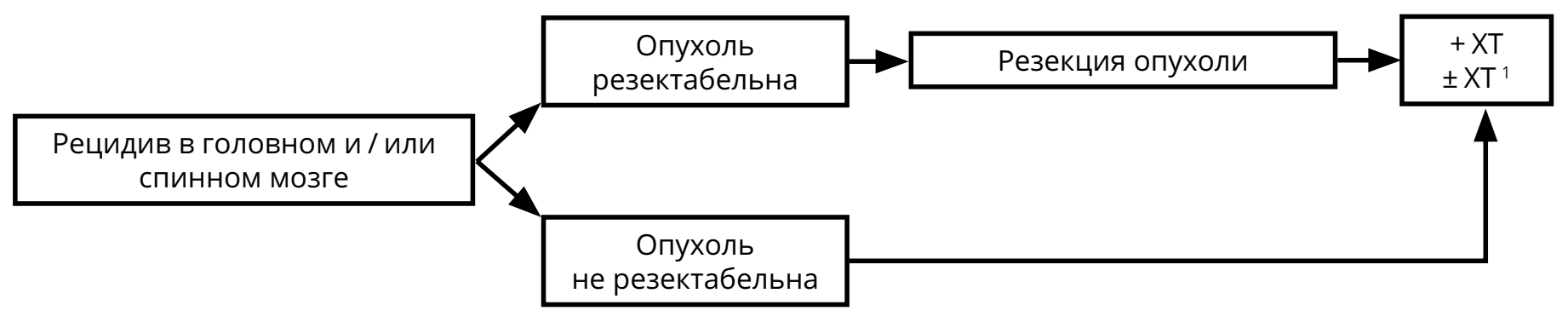
При рецидивах лимфомы ЦНС решение о методе лечения принимается исходя из нескольких параметров: времени с момента первичной верификации, продолжительности ремиссии, общего состояния больного, распространённости опухоли на момент рецидива (рис. 9).
3.3.5. Первичные герминогенные (герминативно-клеточные) опухоли ЦНС
Редкая группа первичных опухолей ЦНС (0,9 % от всех первичных опухолей ЦНС), встречается в основном в детском и молодом возрасте (медиана возраста на момент установления диагноза — примерно 17 лет), преобладает у лиц мужского пола (в соотношении м/ж 7:1). Гистологически все разновидности этих опухолей идентичны аналогичным семиномным и несеминомным опухолям яичка и яичника. Самой частой локализацией первичных герминативно-клеточных опухолей ЦНС является пинеальная область, что обусловливает две типичные группы симптомов: окклюзионно-гидроцефальный синдром и глазодвигательные нарушения. Поскольку негерминогенные герминативно-клеточные опухоли ЦНС характеризуются повышением в плазме крови опухолевых маркёров (АФП и/или β-ХГЧ), при подозрении на данные опухоли обязательно выполнение анализов крови на данные маркёры. Более того, при выявлении клинически значимого повышения одного или обоих маркёров (ХГЧ — более 5 × ВГН, АФП — более 2 × ВГН) лечение начинают без гистологической верификации опухоли с ХТ. По клиническому течению, формирующему подходы к лечению, разделяют герминому (устоялся также термин «чистая герминома» ЦНС) и негерминогенные герминативно-клеточные опухоли. При нормальных уровнях маркёров показана верификация диагноза. В соответствии с Морфологической классификацией ВОЗ опухолей ЦНС 2016 г. выделяют следующие морфологические типы первичных герминативно-клеточных опухолей ЦНС:
опухоль желточного мешка;
тератома со злокачественной трансформацией;
смешанные герминативно-клеточные опухоли.
Помимо маркёров, для полноценной диагностики данной группы опухолей необходимо выполнение МРТ с контрастированием всего головного и спинного мозга. Как и при первичной лимфоме ЦНС, при первичной герминоме ЦНС хирургическое удаление не улучшает прогноз, поэтому СТБ, эндоскопическая или открытая биопсия опухоли предпочтительнее удаления.
3.3.5.1. Первичная («чистая») герминома ЦНС
Современный подход к лечению заключается в ХТ в режиме EP (цисплатин +этопозид) (см. раздел 4) с последующим облучением желудочковой системы головного мозга СОД 24 Гр (при отсутствии данных за метастазирование по оболочкам спинного мозга). Поражение хиазмально-селярной области требует выполнения анализов крови на гормоны гипофиза на всех этапах лечения с участием эндокринолога (лучше — нейроэндокринолога). Краткий алгоритм лечения больных с первичной герминомой ЦНС:
МРТ головного и спинного мозга с контрастированием;
кровь на опухолевые маркёры (АФП, β-ХГЧ) — должны быть в пределах нормы;
обследование у невролога, офтальмолога, эндокринолога;
СТБ или прямая биопсия для верификации диагноза (при необходимости — решение вопроса о ликворошунтирующей операции);
ХТ по схеме EP (цисплатин + этопозид) — каждые 21 день;
после 2 курсов — контрольная МРТ головного и спинного мозга с контрастированием;
после 4 курсов — повторный контроль: МРТ головного и спинного мозга с контрастированием; при полном или «почти полном» эффекте — ЛТ в объёме облучения всей желудочковой системы (до уровня С2 шейного позвонка): РОД 1,8–2,0 Гр, СОД 24 Гр; в случае подозрения на остаточную опухоль (вероятнее всего — зрелую тератому) до ЛТ решается вопрос об удалении;
контрольная МРТ головного и спинного мозга каждые 3 мес. в течение первого года наблюдения, затем — каждые 6 мес. в течение 2‑го и 3‑го годов наблюдения, затем — 1 раз в год или при выявлении неврологических симптомов. Эффективность такого лечения достигает 90 % для 5‑летней и 10‑летней безрецидивной выживаемости, поэтому у фертильных пациентов мужского пола до начала лечения целесообразно решение вопроса о криоконсервации спермы.
3.3.5.2. Первичные негерминогенные герминативно-клеточные опухоли ЦНС
Ещё более редкая, чем первичная герминома ЦНС, группа опухолей, неоднородная по спектру морфологических форм (эмбриональная карцинома, опухоль желточного мешка, хориокарцинома, тератома (незрелая, тератома со злокачественной трансформацией)), с менее благоприятным по сравнению с «чистой» герминомой прогнозом.
Краткий алгоритм лечения больных с первичными негерминогенными герминативно-клеточными опухолями ЦНС:
МРТ головного и спинного мозга с контрастированием;
кровь на опухолевые маркёры (АФП, β-ХГЧ) — как правило, повышены;
обследование у невролога, офтальмолога, эндокринолога;
ХТ по схеме «цисплатин + ифосфамид + этопозид» каждые 21 день;
после 2 курсов — контрольная МРТ головного и спинного мозга с контрастированием, контроль опухолевых маркёров;
после 4 курсов — повторный контроль: МРТ головного и спинного мозга с контрастированием, контроль опухолевых маркёров; при полном или почти полном ответе– ЛТ в объёме краниоспинального облучения: РОД 1,8–2,0 Гр, СОД 36 Гр; в случае подозрения на остаточную опухоль (вероятнее всего — одну из разновидностей тератомы) — до ЛТ необходимо обсудить вопрос об удалении;
контрольная МРТ головного и спинного мозга каждые 3 мес. (+ контроль опухолевых маркёров) в течение первых 2 лет наблюдения, затем — каждые 6 мес. в течение 3‑го и 4‑го годов наблюдения, затем — 1 раз в год или при выявлении неврологических симптомов.
5‑летняя безрецидивная выживаемость при таком режиме лечения составляет 60–70 %.
До начала ХТ — решение вопроса о криоконсервации спермы.
3.4. Режимы лекарственной терапии первичных опухолей ЦНС
Рекомендуемые режимы лекарственной терапии различных вариантов первичных опухолей ЦНС представлены в табл. 1, 2, 3.
| PCV: ломустин 90 мг/м 2 внутрь в 1‑й день +винкристин 1,5 мг/м 2 в/в в 1‑й и 8‑й дни + прокарбазин 70 мг/м 2 внутрь в дни 8–21‑й дни, каждые 6 нед. |
|---|
| Метотрексат 3–8 г/м 2 в/в в 1‑й день (+ кальция фолинат 0,5 мг/кг в/в каждые 6 часов, начиная через 24 часа после введения метотрексата и под контролем снижения его концентрации в крови) + дексаметазон 8 мг/сут. в 1–3‑й дни, каждые 3 нед.; проводится только в стационарных условиях онкогематологического отделения или отделения химиотерапии |
|---|