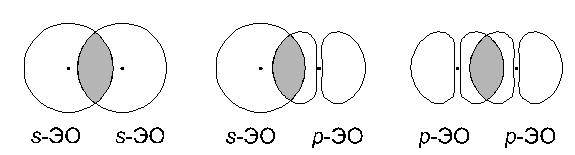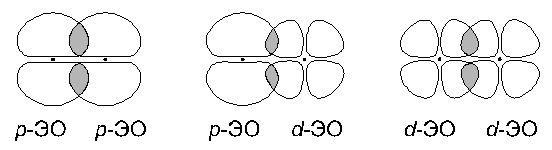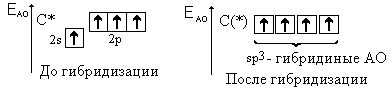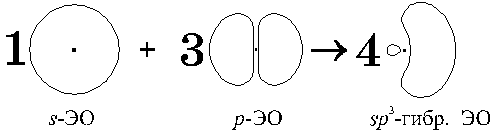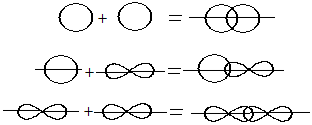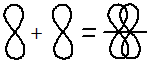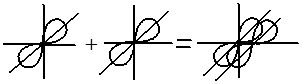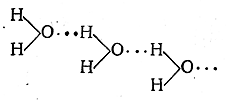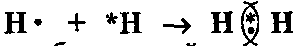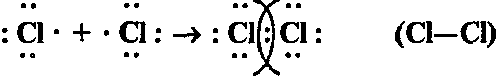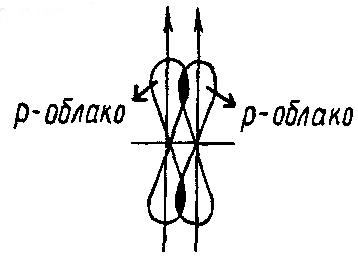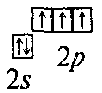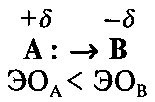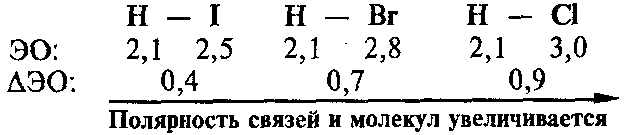что представляет собой область перекрывания электронных облаков
Что представляет собой область перекрывания электронных облаков
7.8. Виды ковалентной связи
Ковалентная связь образуется за счет перекрывания электронных облаков связываемых атомов. Существуют разные способы перекрывания этих электронных облаков.
1. Прямое перекрывание:
В этом случае единственная область перекрывания электронных облаков лежит на прямой, соединяющей ядра атомов. Связь, образованная таким образом, называется 
В зависимости от вида перекрывающихся облаков может образоваться 




2. Боковое перекрывание:
В этом случае две области перекрывания электронных облаков находятся по разные стороны от плоскости, в которой лежат ядра связываемых атомов. Связь, образованная при таком перекрывании ЭО, называется 
Как и в случае 





И 





Одна область перекрывания
Две области перекрывания
Электронные облака перекрываются частями с наибольшей электронной плотностью
Перекрывание эффективное
Связь прочная
Электронные облака перекрываются своими периферийными частями
Перекрывание менее эффективное
Связь менее прочная
Так как 




| Циановодород – HCN. Другое название – синильная кислота. Это бесцветная летучая жидкость с температурой кипения 26 o С. При сильном нагревании или на свету она разлагается. Синильная кислота смешивается с водой во всех отношениях. По аналогии с галогеноводородами раствор циановодорода в воде называют циановодородной кислотой. Синильная кислота и ее соли (цианиды) – очень сильные яды (смертельная доза для человека не более 50 мг), причем сама кислота способна проникать в организм даже через неповрежденную кожу. Попав в организм, циановодород и цианиды связывают гемоглобин в циангемоглобин, поражают дыхательные центры и вызывают удушье. Несмотря на свою токсичность, синильная кислота используется в производстве синтетических волокон и некоторых видов пластмасс. В небольших концентрациях синильная кислота встречается в растительном мире (например, в горьком миндале). |


2.Составьте обычные структурные и электронные формулы следующих веществ: CH3Cl, COF2, SO2Cl2 и N2H4. В случае затруднения изобразите схемы образования связей в этих молекулах. Укажите в структурных формулах 

7.9. Энергия ковалентной связи
Прочность связи характеризуется энергией связи (см. параграф 7.5). Прочность ковалентной связи можно оценить двумя способами: определив энергию, необходимую для разрыва всех связей в определенной порции вещества, или определив энергию, необходимую для разрыва известного числа связей. В первом случае такая энергия называется энергией атомизации, во втором – энергией связи. На практике используют соответствующие молярные величины.
| Молярная энергия атомизации (Еат) – отношение энергии, затрачиваемой на разделение порции молекул вещества на изолированные атомы, к количеству вещества в этой порции. |
Молярная энергия атомизации показывает, какую энергию нужно затратить на разделение 1 моля вещества на изолированные атомы.
| Молярная энергия связи (Есв) – отношение энергии, затрачиваемой на разрыв определенного числа связей, к числу этих связей, измеренному в молях. |
Таблица 21.Примеры значений Еат и средних значений Есв (в кДж/моль)
Из приведенных в таблице 21 значений можно сделать вывод, что прочность ковалентных связей тем больше, чем меньше размеры связываемых атомов и больше кратность связи.

7.10. Строение молекул. Модель гибридизации
Большинство соединений с ковалентными связями между атомами состоит из молекул.
Понятие » строение молекул» – довольно широкое понятие и включает в себя, в частности, химическое строение и пространственное строение.
| Химическое строение молекулы – последовательность и тип связей между атомами в молекуле. |
Химическое строение молекулы описывается структурной формулой.
Пространственное строение молекулы – взаимное расположение атомов молекулы в пространстве.
Пространственное строение молекулы описывается пространственной формулой.
Чтобы охарактеризовать пространственное строение молекулы количественно, нужно определить межатомные расстояния и углы между связями. И то, и другое может быть определено экспериментально.
Межатомное расстояние – расстояние между ядрами атомов.
Угол между связями – угол между прямыми, проходящими через ядра атомов, связанных ковалентными связями.
Для оценки межатомных расстояний в молекулах веществ, пространственное строение которых еще не изучено, часто используют так называемые атомные (ковалентные) радиусы.
Атомный радиус – половина расстояния между атомами, связанными простой связью, в молекуле или кристалле простого вещества.
Сумма атомных радиусов атомов разных элементов равна среднему расстоянию между атомами этих элементов, связанными простой ковалентной связью, в молекулах или кристаллах. Таблица атомных радиусов приведена в приложении 9.
Для оценки углов между связями оказывается полезной модель гибридизации.
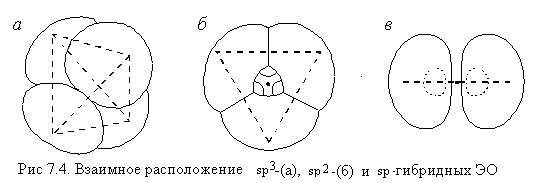
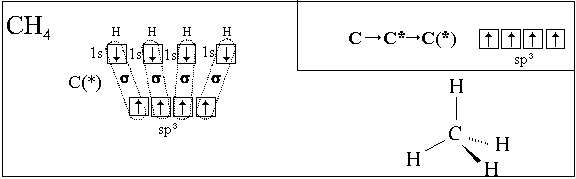
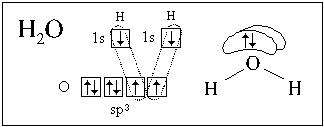
Вспомним химическое строение молекулы метана (см. рис. на стр. 21). Из схемы образования ковалентных связей в этой молекуле (стр. 105) следует, что три из четырех связей в этой молекуле совершенно одинаковы. Так как оси электронных облаков p-АО взаимно перпендикулярны, то и три ковалентных связи, образованные с участием этих облаков, должны быть направлены под прямым углом друг к другу. Четвертая же связь должна от них несколько отличаться. Экспериментально установлено, что все четыре связи в молекуле метана совершенно одинаковы и направлены в пространстве так, как это показано на рисунке (стр. 21). То есть атом углерода занимает положение в центре тетраэдра (правильного четырехгранника, треугольной пирамиды), а атомы водорода – в его вершинах. Это возможно только в том случае, если электронные облака атома углерода, участвующие в образовании связи, совершенно одинаковы и соответствующим образом расположены в пространстве.
В рамках модели гибридизации предполагается, что такое выравнивание действительно происходит.
| Гибридизация атомных орбиталей и электронных облаков – предполагаемое выравнивание атомных орбиталей по энергии, а электронных облаков по форме при образовании атомом ковалентных связей. |
Электронные облака 2s- и 2р-орбиталей меняют свою форму – они тоже выравниваются:
Форма гибридных ЭО допускает только прямое перекрывание этих облаков с облаками других атомов, поэтому с участием гибридных АО могут образовываться только 
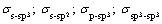
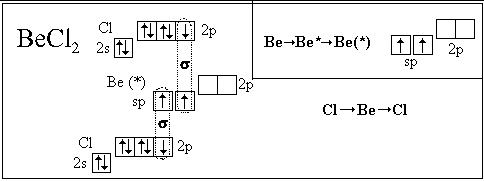
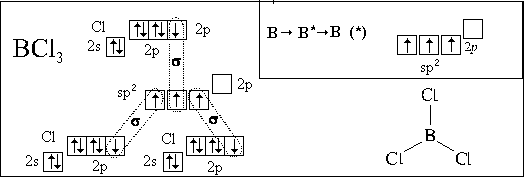
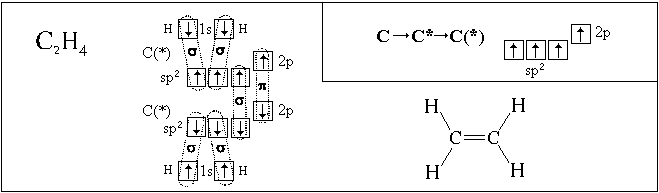
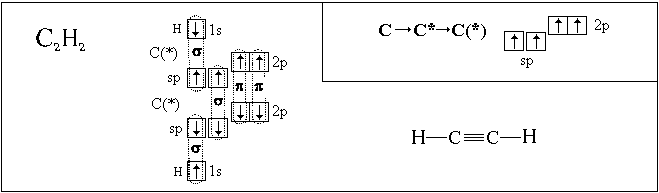
Посмотрим, как с использованием модели гибридизации описывается пространственное строение некоторых молекул:
Полученные нами пространственные формулы хорошо согласуются с экспериментальными данными.
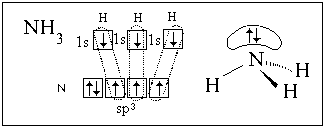
В приведенных примерах гибридизации подвергались только орбитали с неспаренными электронами. Но, если на валентных подуровнях атома часть орбиталей полностью заполнена, эти АО тоже участвуют в гибридизации. Так гибридизуются валентные орбитали атома азота в аммиаке и атома кислорода в воде.


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
Способы перекрывания электронных облаков



1. Вдоль межъядерной оси – сигма связь (σ)
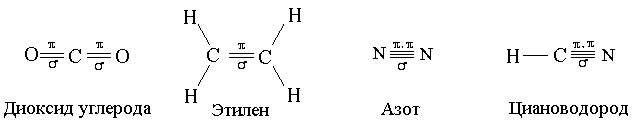
Следует различать понятия «полярность связи» и «полярность молекулы». Например, и σ- и π- связь С=О полярны, а молекула СО2 неполярна, т.к. суммарный дипольный момент молекулы равен нулю.
Ионная связь.Такой тип химической связи возникает только при взаимодействии атомов, которые сильно отличаются по электроотрицательности, т.е. между типичными металлами и типичными неметаллами.
При химическом взаимодействии типичные металлы, имеющие на внешнем энергетическом уровне 1 – 2 электрона, отдают их атому неметалла, который приобретает завершённый энергетический уровень и превращается в отрицательно заряжённый ион, а атом, отдавший электроны – в положительно заряженный ион. Например NaCl:
Сl 0 1s 2 2s 2 2p 6 3s 2 3p 5 + е → Сl ¯ 1s 2 2s 2 2p 6 3s 2 3p 6
Между образовавшимися ионами осуществляется электростатическое взаимодействие, приводящее к образованию химического соединения. Химическая связь между ионами, осуществляемая электростатическим притяжением, называется ионной или электровалентной связью.
Соединения, которые образовались за счёт притяжения ионов, называются гетерополярными или ионными. Ионные соединения состоят из молекул только в парообразном состоянии.
Металлическая связь – сильно делокализованная химическая связь. Возникает в том случае, когда атомы имеют мало валентных электронов по сравнению с количеством свободных валентных орбиталей, валентные электроны слабо удерживаются ядром из – за малой энергии ионизации. Наличие в металле так называемых свободных электронов (электронного газа) характеризует многие общие для всех металлов свойства: металлический блеск, теплопроводность и электрическую проводимость.
Свободные электроны связывают друг с другом ионы.
Данный вид связи характерен для металлов и их сплавов, а так же для интерметаллических соединений, она ненасыщенна и ненаправлена.
Водородная связь. Межмолекулярное взаимодействие может осуществляться не только за счёт донорно – акцепторных связей, но и за счёт сил Ван-дер-Ваальса (дисперсионного, ориентационного и индукционного взаимодействия) и водородной связи. Водородная связь обусловлена тем, что атом водорода, химически связанный в одной молекуле с атомом высокой элктроотрицательностью (например, фтора, кислорода) может соединиться ещё с атомом этого же элемента из другой молекулы. Водородную связь обозначают пунктиром
Водородная связь менее прочна чем обычная химическая связь, но оказывает влияние на многие свойства веществ. Различают межмолекулярную водородную связь и внутримолекулярную.
Контрольные задания.
99-118. Укажите тип химической связи в молекулах соединений вашего варианта. Составьте электронные схемы образования молекул с ковалентной связью. Электроны каких орбиталей атомов принимают участие в образовании ковалентной связи? Определите валентность и степени окисления атомов в молекуле. Изобразите электронными уравнениями процессы образования ионов из атомов для соединений с ионной связью.
Химическая связь
Разные вещества имеют различное строение. Среди них только благородные газы – гелий, неон, аргон, криптон, ксенон и радон – существуют в виде свободных (изолированных) атомов. Это обусловлено высокой устойчивостью их электронных структур (электронный дублет 1s 2 у Не и электронный октет ns 2 np 6 на внешнем слое в атомах остальных благородных газов).
Все другие вещества состоят из связанных атомов. Силы, которые обусловливают связь между атомами, получили название «химическая связь». По своей природе эти силы являются электростатическими. Они представляют собой различные виды взаимодействия электрических зарядов (электронов и ядер взаимодействующих атомов).
Результатом связывания атомов является образование более сложных структур — молекул, молекулярных ионов, свободных радикалов, а также ионных, атомных и металлических кристаллических решеток.
Существование этих структур обусловлено различными типами химической связи. Важнейшие из них: ковалентная, ионная, металлическая, водородная связи.
Ковалентная связь является причиной образования большинства молекул, молекулярных ионов, свободных радикалов и атомных кристаллических решеток.
Ионная связь обусловливает существование молекул ионных соединений и ионных кристаллических решеток.
Металлическая связь существует в простых веществах — металлах.
Водородная связь существует внутри молекул отдельных веществ, а также возникает между молекулами некоторых веществ.
Ковалентная связь
При образовании химической связи между атомами главную роль играют их валентные электроны, т. е. электроны, которые находятся на внешнем электронном слое и наименее прочно связаны с ядром атома.
Как уже было отмечено, самыми устойчивыми являются внешние электронные оболочки благородных газов (1s 2 и ns 2 nр 6 ). Атомы других элементов при образовании молекул стремятся приобрести устойчивую восьмиэлектронную (октет) или двухэлектронную (дублет) оболочки. Каким образом это происходит?
В 1916 г. Г. Н. Льюис (США) высказал мысль о том, что химическая связь возникает в результате образования общих электронных пар между взаимодействующими атомами. Эта идея легла в основу теории ковалентной связи.
Рассмотрим сущность этой теории на примере образования простейшей молекулы — молекулы водорода Н2.
Таким образом, в образующейся молекуле каждый атом водорода имеет два электрона, следовательно, приобретает устойчивую электронную структуру ls 2 (как у атома гелия). Общую электронную пару в графических формулах молекул показывают в виде черточки: Н—Н.
Любая молекула является устойчивой только в том случае, если при ее образовании из атомов происходит уменьшение полной энергии системы. Поэтому образование химической связи — это процесс, который сопровождается выделением энергии.
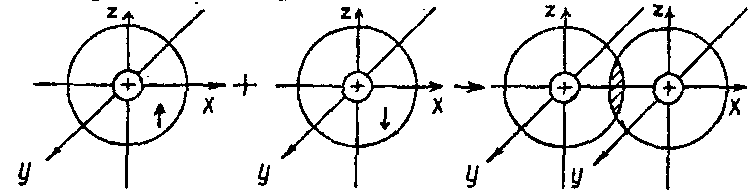
Энергия системы из двух сближающихся атомов водорода, которые имеют электроны с параллельными спинами, при уменьшении расстояния между атомами увеличивается, т. е. образования устойчивой молекулы не происходит. Если же атомы имеют электроны с антипараллельными спинами, то при сближении атомов энергия понижается и достигает минимума при расстоянии между ядрами атомов r0 = 0, 74Å. Следовательно, таково расстояние между ядрами атомов водорода в образующейся устойчивой молекуле H2. Эта величина меньше суммы двух атомных радиусов (0,53Å + 0,53Å = l,06Å).
Отсюда был сделан вывод о том, что при образовании ковалентной связи происходит перекрывание облаков электроинов, имеющих антипараллельные спины.
Область перекрывания электронных облаков — это область высокого отрицательного заряда, который притягивает положительно заряженные ядра атомов.
Схематично перекрывание электронных облаков в молекуле Н2 можно изобразить так:
Один из р-электронов в атоме хлора является неспаренным. При образовании молекулы неспаренные электроны двух атомов хлора образуют одну общую электронную пару; в результате каждый атом хлора приобретает электронную структуру 3s 2 3p 6 (октет):
Перекрывание электронных облаков показано на этом рисунке:
Если между двумя атомами образуется только одна общая электронная пара, то такая ковалентная связь называется одинарной (простой) связью.
Следовательно, связи в молекулах Н2 и Сl2 являются одинарными (простыми) связями.
Как видно из рисунков области перекрывания электронных облаков в молекулах Н2 и Сl2 находятся на линии, которая соединяет ядра атомов.
Ковалентные связи, при образовании которых область перекрывания электронных облаков находится на линии, соединяющей ядра атомов, называются σ-связями (сигма-связями).
Следовательно, связи в молекулах Н2 и Cl2 представляют собой σ-связи.
Одинарные связи всегда являются σ-связями.
Другой разновидностью ковалентных связей являются π-связи.
π-Связи — это ковалентные связи, при образовании которых область перекрывания электронных облаков находится по обе стороны от линии, соединяющей ядра атомов.
s-облака не могут образовывать π-связи. В образовании π-связей могут участвовать р- и d-облака.Например, π-связь образуется при перекрывании двух р-облаков, как это показано на этом рисунке.
π-Связи образуются в тех случаях, когда между двумя атомами возникают две или три общие электронные пары.
Число общих электронных пар между связанными атомами характеризует кратность связи.
Если связь между двумя атомами образована двумя общими электронными парами, то такая связь называется двойной связью. Любая двойная связь состоит из одной σ-связи и одной π-связи: А = В.
Если связь между двумя атомами образована тремя общими электронными парами, то такая связь называется тройной связью. Любая тройная связь состоит из одной σ-связи и двух π-связей: А≡В.
Двойные и тройные связи имеют общее название: кратные связи.
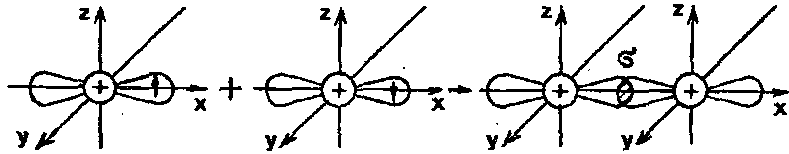
Образование кратных связей рассмотрим на примере молекулы азота N2.
Электронная формула внешнего слоя атома азота: 2s 2 2p 3 электронно-графическая формула:
Три р-электрона в атоме азота являются неспаренными и участвуют в образовании трех общих электронных пар:
Важной характеристикой ковалентной связи является полярность связи.
Полярность связи зависит от электроотрицательности элементов, атомы которых участвуют в образовании связи.
Напомним, что электроотрицательность (ЭО) элемента характеризует способность его атома в молекуле притягивать к себе общую электронную пару.
Если ковалентная связь образуется между атомами с одинаковой ЭО, то общая электронная пара (область перекрывания электронных облаков) находится на одинаковом расстоянии от ядер обоих атомов. Такая связь называется неполярной связью. Неполярные связи существуют в молекулах простых веществ: Н2, N2, Cl2, О2 и т. д.
Молекулы с неполярными связями являются неполярными молекулами.
Если ковалентная связь образуется между атомами с различной ЭО, то общая электронная пара (область перекрывания электронных облаков) смещается в сторону атома с большей ЭО:
В результате смещения электронной плотности на атоме с большей ЭО возникает избыточный отрицательный заряд (—δ), а на атоме с меньшей ЭО — положительный заряд (+δ).
Ковалентная связь с неравномерным распределением электронной плотности между взаимодействующими атомами называется полярной связью.
Если молекула состоит из двух атомов, которые связаны полярной связью, то такая молекула является полярной молекулой, т. е. представляет собой диполь.
Диполь — это электронейтральная система, в которой центры положительного и отрицательного зарядов находятся на определенном расстоянии друг от друга.
Схематично диполь изображается следующим образом:
Расстояние между центрами зарядов называется длиной диполя (l).
Количественной характеристикой полярности связей и молекул является дипольный момент.
Дипольный момент равен произведению заряда 5 на длину диполя l:
μ = δ∙l
Чем больше дипольный момент, тем больше полярность связи и молекулы. Дипольный момент является векторной величиной. Вектор дипольного момента направлен от центра положительного заряда к центру отрицательного заряда.
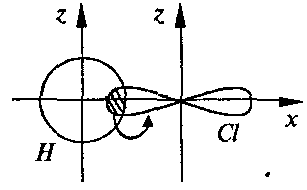
Примером полярной молекулы является молекула хлороводорода НCl.
В результате перекрывания s-облака атома водорода и р-облака атома хлора образуется одинарная σ-связь:
Так как ЭО хлора больше ЭО водорода, связь в молекуле НCl является полярной связью. Следовательно, молекула HCl представляет собой диполь.
Чем больше разность ЭО связанных атомов, тем сильнее смещается электронная плотность к атому более электроотрицательного элемента, тем больше дипольный момент молекулы. Например, в ряду молекул НI→HBr→HCl разность ЭО и полярность связей и молекул увеличиваются:
Если молекула состоит из трех или большего числа атомов, дипольный момент молекулы равен векторной сумме дипольных моментов всех связей в этой молекуле.
Для определения дипольного момента молекулы необходимо знать расположение в пространстве векторов дипольных моментов связей, которое зависит от геометрического строения молекулы.
Скачать:
Скачать бесплатно реферат на тему:» Основные типы химической связи» Основные-типы-химической-связи.docx (179 Загрузок)
Рефераты по другим темам можно скачать здесь