что препятствует слипанию стенок альвеол
Лёгочный сурфактант
Сурфакта́нт (в переводе с английского — поверхностно-активное вещество [1] ) — смесь поверхностно-активных веществ, находящаяся на границе воздух-жидкость в лёгочных альвеолах, то есть выстилающая альвеолы изнутри. Препятствует спадению (слипанию) альвеол за счёт снижения поверхностного натяжения жидкости. Сурфактант секретируется специальной разновидностью альвеолоцитов II типа.
Содержание
Состав
Состав лёгочного сурфактанта [2] :
Свойства
Сурфактант синтезируется и секретируется пневмоцитами (альвеолоцитами) II типа. За счёт поверхностно-активного натяжения сурфактант понижает поверхностное натяжение в альвеоле, предупреждая её «спадение». Сурфактант также имеет защитное действие. Высокие поверхностно-активные свойства сурфактанта объясняются присутствием в нём дипальмитоилфосфатидилхолина, который образуется в лёгких доношенного плода непосредственно перед родами.
Система сурфактантов у недоношенных детей не развита, что часто является причиной гибели недоношенных детей без лечения. Система сурфактанта может повреждаться и у взрослых при травмах, в том числе химических и термических, а также при некоторых заболеваниях.
Сурфактант помогает лёгким всасывать, усваивать кислород. В последнее время мода на безжировое питание приводит к возникновению гипоксий у людей, которые не употребляют в пищу качественные жиры. В то же время сурфактант примерно на 90% состоит из жиров.
Строение
Располагающийся на поверхности альвеолярного эпителия сурфактант включает 2 фазы:
Гипофаза
Нижняя, состоит из тубулярного миелина, имеющего решетчатый вид и сглаживающего неровности эпителия.
Апофаза
Поверхностная мономолекулярная плёнка фосфолипидов, обращённая в полость альвеолы гидрофобными участками.
Функции
Примечания
См. также
Литература
Ссылки
Полезное
Смотреть что такое «Лёгочный сурфактант» в других словарях:
Лизофосфатидилхолинацилтрансфераза — Лизофосфатидилхолин ацилтрансфераза 1 Обозначения Символы AYTL2; LPCAT Entrez Gene … Википедия
ЗАБОЛЕВАНИЯ ЛЁГКИХ ХРОНИЧЕСКИЕ ОБСТРУКТИВНЫЕ — мед. Хронические обструктивные заболевания лёгких (ХОЗЛ) хроническая патология с прогрессирующей обструкцией дыхательных путей и развитием лёгочной гипертёнзии. Термин объединяет хронический обструктивный бронхит и эмфизему. • Хронический бронхит … Справочник по болезням
лёгкие — их; мн. (ед. лёгкое, ого; ср.). Орган дыхания (у человека и позвоночных животных), расположенный в грудной полости. Обследовать л. Рентген лёгких. Объём лёгких. Дышать лёгкими. ◁ Лёгочный, ая, ое. Л ая ткань. Л ая артерия. Л ые болезни. * * *… … Энциклопедический словарь
Острый респираторный дистресс-синдром — Рентгенограмма … Википедия
Бронхолегочная дисплазия и кислородная зависимость у недоношенных детей
Что это? Как лечить? Чем может помочь фонд?
Бронхолегочная дисплазия – одно из самых распространенных заболеваний недоношенных малышей. На важные вопросы о БЛД отвечаем вместе с экспертами «Право на чудо» – докторами медицинских наук Мариной Викторовной Нароган и Дмитрием Юрьевичем Овсянниковым, а также и к. м. н, врачом-неонатологом высшей категории Анной Львовной Карповой.
Что такое бронхолегочная дисплазия?
Слово «дисплазия» означает нарушение формирования. При бронхолегочной дисплазии (БЛД) нарушено правильное развитие бронхов. Это происходит потому, что у недоношенного ребенка легкие начинают дышать раньше, чем легочная ткань успевает созреть для нормального газообмена.
! Чем раньше родился ребенок, тем выше вероятность бронхолегочной дисплазии.
Что происходит при БЛД?
Стенки дыхательных пузырьков – альвеол – становятся толще, медленнее насыщают кровь кислородом и хуже выводят углекислый газ. То есть, легкие не могут нормально справляться со своей функцией. Дыхательные пути становятся более жесткими, сужаются.
Как проявляется БЛД, какие могут быть последствия?
У ребенка возникает одышка, он тяжело и часто дышит. Насыщенность кислородом крови ниже, чем у здоровых детей. В результате ребенок долго нуждается в дополнительном кислороде или не может отказаться от искусственной вентиляции легких.
Среди осложнений БЛД – легочная гипертензия (перегрузка сердца из-за высокого давления в легочной артерии), тяжелые ОРЗ в первые годы жизни, склонность к бронхообструкциям, высокие риски пневмонии и астмы.
Лечение и профилактика
Современные методы профилактики БЛД – это:
Благодаря современным методам лечения и профилактики тяжелые формы бронхолегочной дисплазии встречаются все реже. Однако число БЛД год от года растет, так как растет выживаемость недоношенных детей.
Зачем детям с БЛД назначают дополнительный кислород?
У здоровых доношенных детей средний уровень сатурации (насыщение крови кислородом) в течение первого года жизни составляет 97–98%.
У недоношенных детей с бронхолегочной дисплазией концентрация кислорода в крови часто менее 94%.
Таким детям для дыхания и нормальной работы организма недостаточно обычного комнатного воздуха – и врач назначает кислород дополнительно.
В большинстве случаев кислородотерапия может проводиться в домашних условиях. Зависимые от кислорода дети, которые не нуждаются в круглосуточном нахождении в стационаре, могут быть выписаны – если дома у них будет возможность самостоятельно проводить кислородотерапию.
Как долго ребенок может нуждаться в дополнительном кислороде дома, от чего это зависит?
У детей с бронхолегочной дисплазией средняя продолжительность кислородотерапии составляет 12–15 месяцев. После отлучения от кислорода детям может потребоваться дополнительный кислород во время обострения основного заболевания или при инфекционных заболеваниях.
Решение о начале и прекращении кислородотерапии всегда принимает врач. Пациенты, получающие кислород на дому, должны находиться под наблюдением педиатра и пульмонолога.
Как часто ребенку с БЛД нужен дополнительный кислород в течение дня?
Это зависит от уровня насыщения кислородом в крови у ребенка в течение дня. Некоторым детям дополнительный кислород требуется только тогда, когда они активны, или только во время ночного или дневного сна (эпизоды бессимптомного снижения сатурации чаще всего возникают во сне). В других случаях ребенку требуется дополнительный кислород непрерывно.
Как влияет домашняя кислородотерапия на ребенка?
Что должны знать и уметь родители ребенка, которому назначили домашнюю кислородотерапию?
Перед выпиской кислородозависимого ребенка из больницы родителей обучают:
1) правилам использования кислородного оборудования. Например: стационарный кислородный концентратор не должен располагаться близко к пациенту, так как он нагревается и шумит – ребенку может быть некомфортно.
Оборудование должно работать в хорошо проветриваемом помещении, рядом нельзя курить, использовать аэрозоли, фен, располагать отопительные приборы, т.к. кислород – огнеопасный газ.
Родители должны уметь самостоятельно менять/мыть фильтр, который предохраняет концентратор от попадания в него пыли и грязи, доливать ежедневно воду в колбу для увлажнения воздуха, вовремя менять и дезинфицировать кислородную маску, носовые канюли и так далее.
2) также родители учатся измерять сатурацию (насыщение крови кислородом) с помощью пульсоксиметра. Необходимо, чтобы уровень кислорода в крови был не ниже 92% у детей без легочной гипертензии и выше 94% у больных с легочной гипертензией.
3) обязательно знать о симптомах гипоксемии (недостаточного уровня кислорода в организме ребенка). Симптомами недостатка кислорода у ребенка могут быть:
4) родители должны знать основы сердечно-легочной реанимации и уметь оказать первую помощь своему ребенку до приезда медицинских работников.
Где семьи недоношенных детей с бронхолегочной дисплазией могут получить дополнительную помощь?
В фонде «Право на чудо» действует программа «Кислород». Мы закупаем и предоставляем семьям недоношенных детей с тяжелой формой бронхолегочной дисплазии кислородное оборудование в безвозмездную аренду, чтобы ребёнок мог поехать из больницы домой.
Амбробене от кашля назначается повсеместно, переносится хорошо. Мы в данной статье рассмотрим безрецептурные формы препарата: таблетки, сироп, раствор для ингаляций и приема внутрь.
Важно! Самостоятельно выбирать лекарство мы не рекомендуем, поскольку человеку трудно определить, какой тип кашля у него присутствует, и не только по этой причине. Опасным осложнением инфекций дыхательных путей является пневмония (воспаление легких). Она может протекать почти без кашля и без высокой температуры, в итоге пациент начинает лечиться сам и теряет драгоценное время. Лучше сразу посетить терапевта, исключить пневмонию и коронавирус, и только после этого покупать лекарства.
Лекарственные формы препарата Амбробене
Форму Амбробене подбирает врач. Таблетки обычно назначают взрослым для приема трижды в день. Капсулы с пролонгированным действием созданы для тех, кто может принимать лекарство только один раз в день. Растворы для ингаляций и приема внутрь показаны в более трудных случаях, когда важна высокая скорость всасывания. Для детей предусмотрен Сироп.
Важно! Эффект всех препаратов Амбробене проявляется при условии потребления большого количества жидкости, поэтому необходимо обильное питье в ходе терапии. Нельзя сочетать Амбробене с препаратами, подавляющими кашлевой рефлекс (средства от сухого кашля) во избежание застоя мокроты.
Амбробене сироп
Сироп назначают детям. Он содержит амброксол 15 мг в 5 мл, дозирование производится с помощью мерного стаканчика. Родители должны следить за тем, чтобы ребенок принимал много жидкости в ходе приема препарата, иначе эффекта не будет. Если врач не назначил, лечение ведут не более 4-5 дней. Сироп принимают после еды.
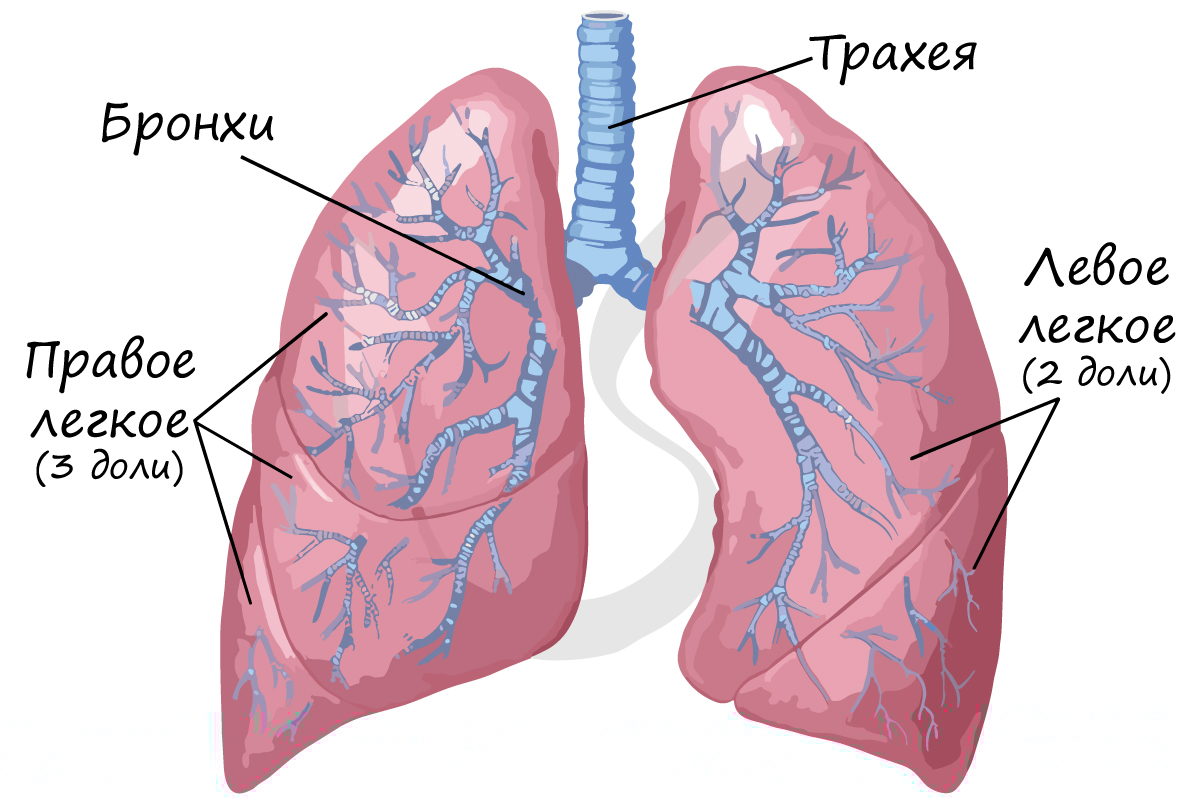
Легкие
Строение легких
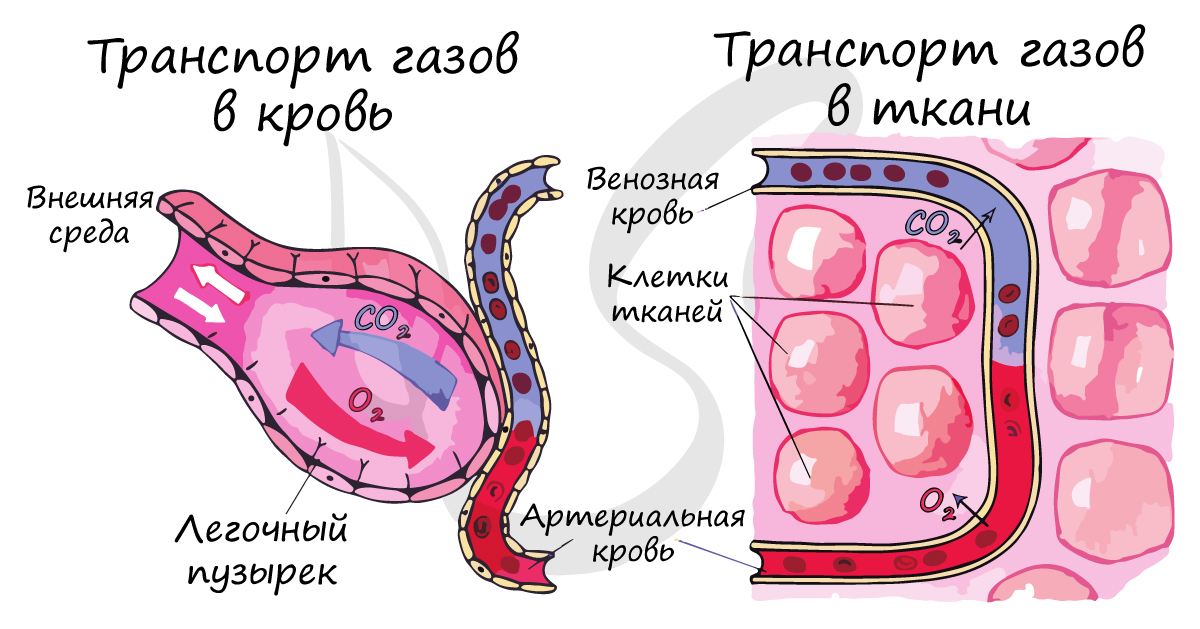
Газообмен в легких и тканях
Соединение гемоглобина с угарным газом гораздо устойчивее, чем остальные: угарный газ легко выигрывает в конкуренции с кислородом и занимает его место. Этим объясняются тяжелые последствия отравлений угарным газом, который быстро скапливается при пожаре в замкнутом помещении.
По мере того, как кровь отдает углекислый газ и принимает кислород, из венозной крови (бедной кислородом) она превращается в кровь артериальную. В тканях происходит обратный процесс: клетки нуждаются в кислороде, необходимом для тканевого дыхания, а углекислый газ, побочный продукт обмена веществ, требует удаления из клетки в кровь.
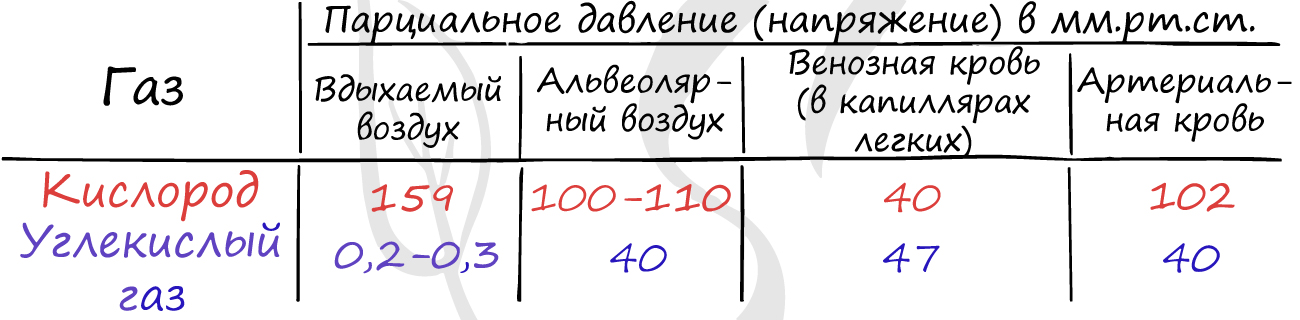
Парциальным давлением газа называют ту часть от общего объема газа, которая приходится на долю данного газа. Не рекомендую вам заучивать таблицу, приведенную выше, но для понимания она весьма хороша.
Жизненная емкость легких
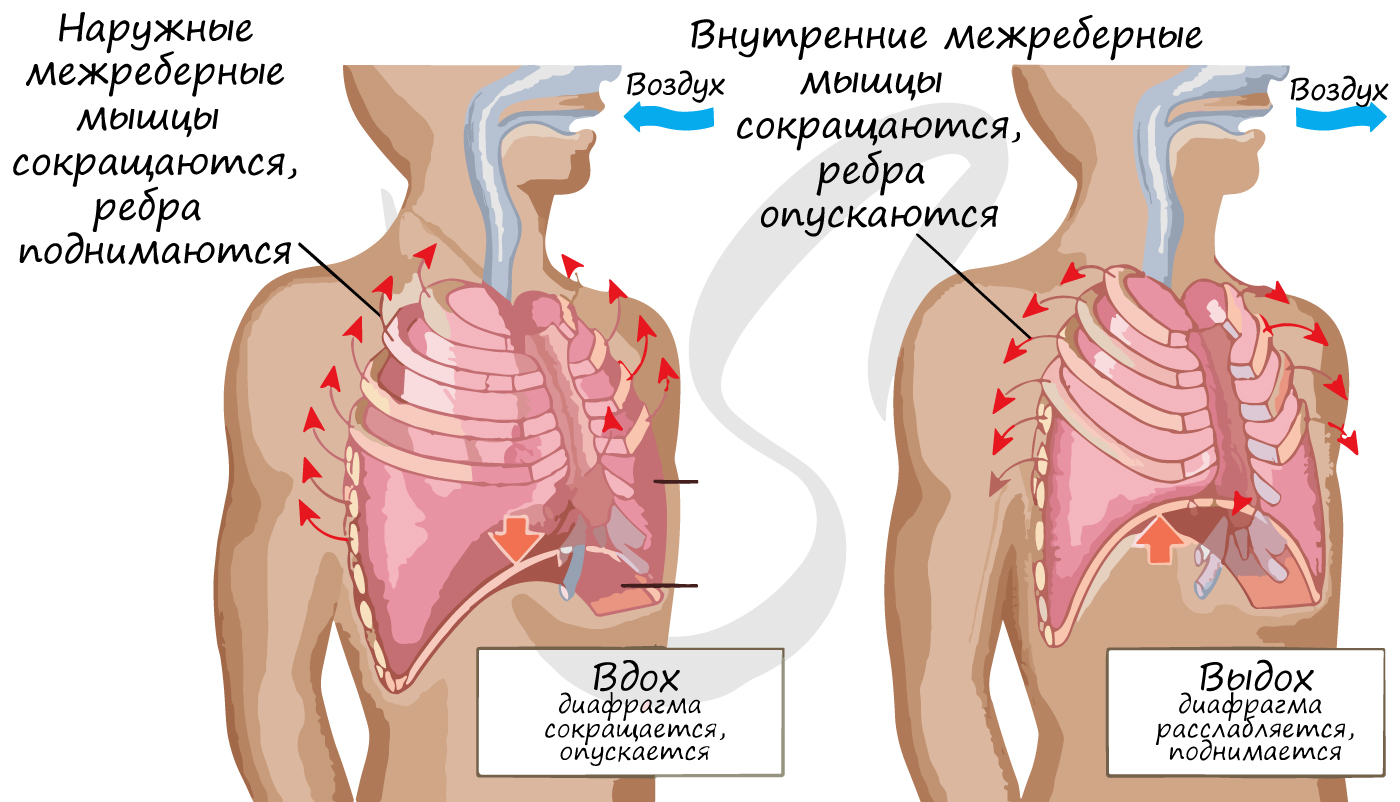
Механизм легочного дыхания
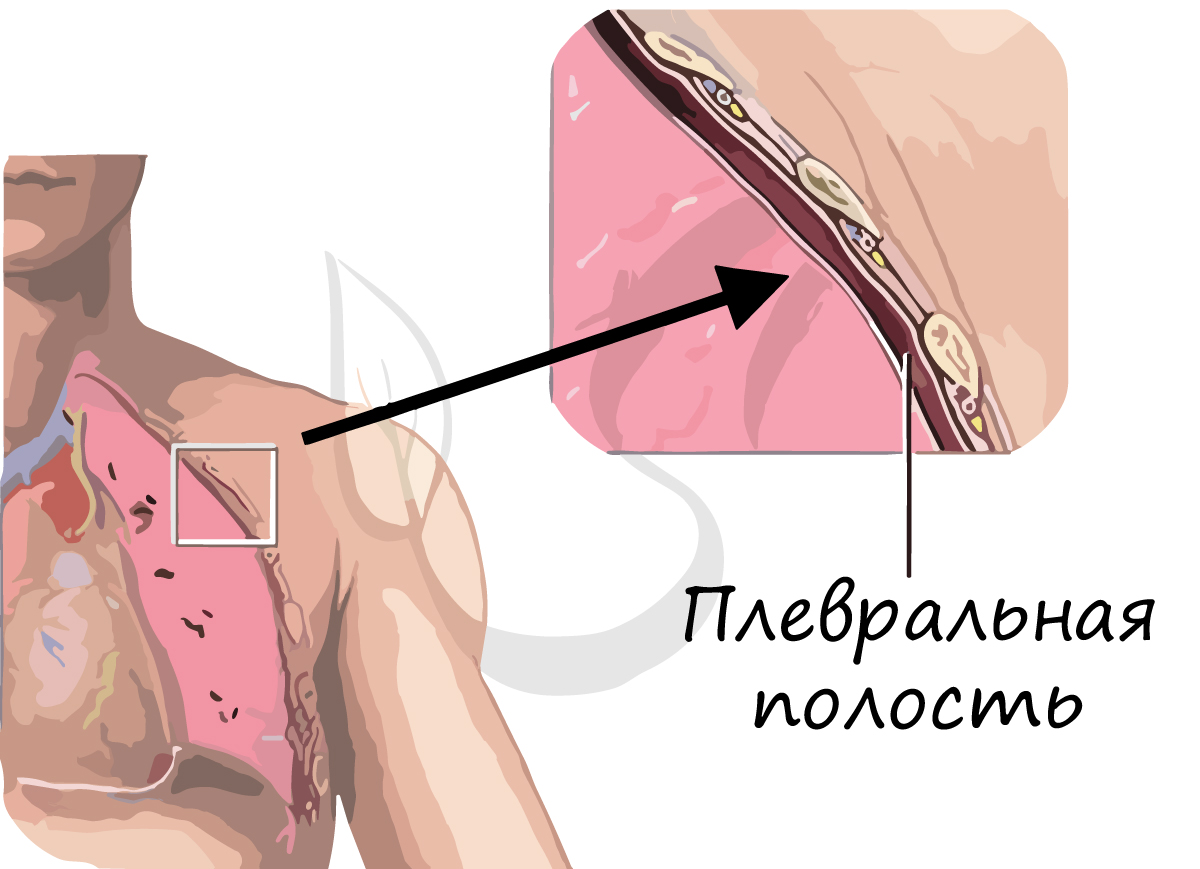
Между наружной поверхностью легкого и стенками грудной клетки имеется плевральная полость, которая играет важнейшую роль в процессе вдоха и выдоха, а также уменьшает трение легких при дыхательных движениях.
Давление в плевральной полости всегда ниже на 5-7 мм. рт. ст. атмосферного давления, поэтому легкие постоянно находятся в расправленном состоянии, скреплены через плевру со стенками грудной полости.
Вообразите: легкое подтягивается к плевре, которая скреплена с грудной клеткой. А грудная клетка постоянно совершает дыхательные движения, расширяясь и сужаясь, таким образом, легкое следует за дыхательными движениями грудной клетки.
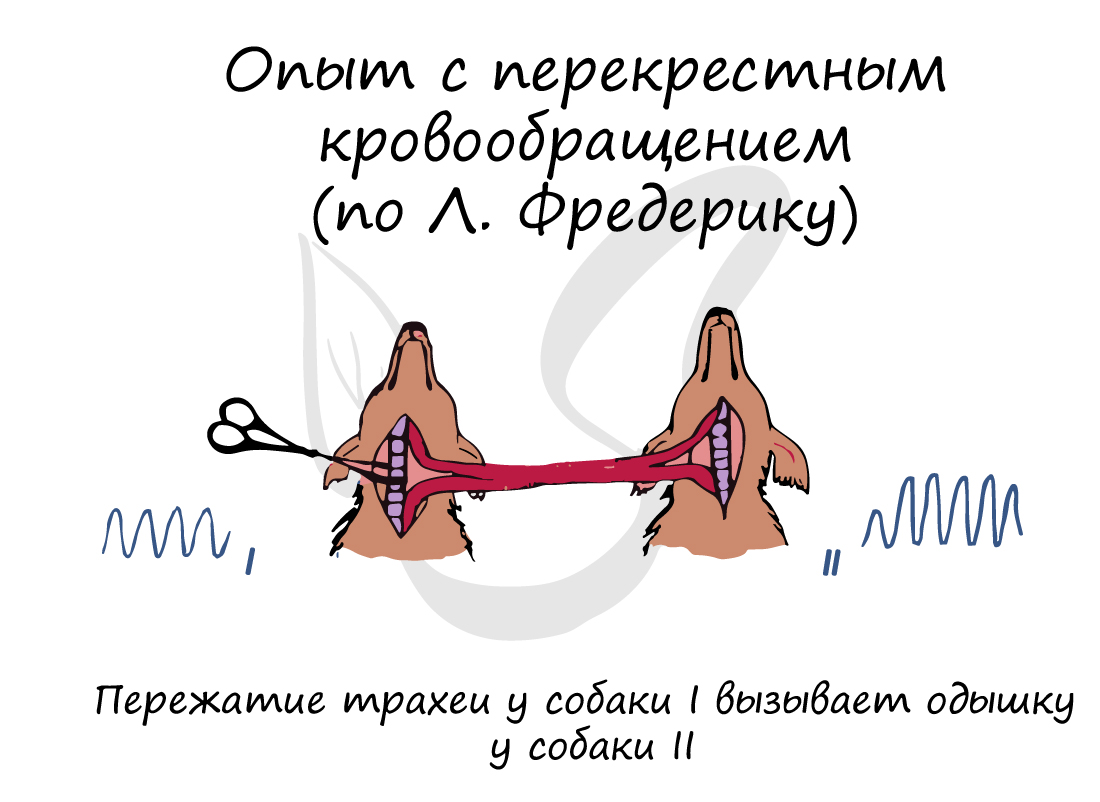
Состав крови сильно влияет на интенсивность дыхания. В многочисленных опытах было выявлено, что увеличение концентрации CO2 возбуждает дыхательный центр. Этим можно объяснить учащение дыхания во время физической нагрузки, к примеру, бега, когда в клетках мышц ног идет активное образование CO2 и поступление его в кровь, дыхание учащается рефлекторно.
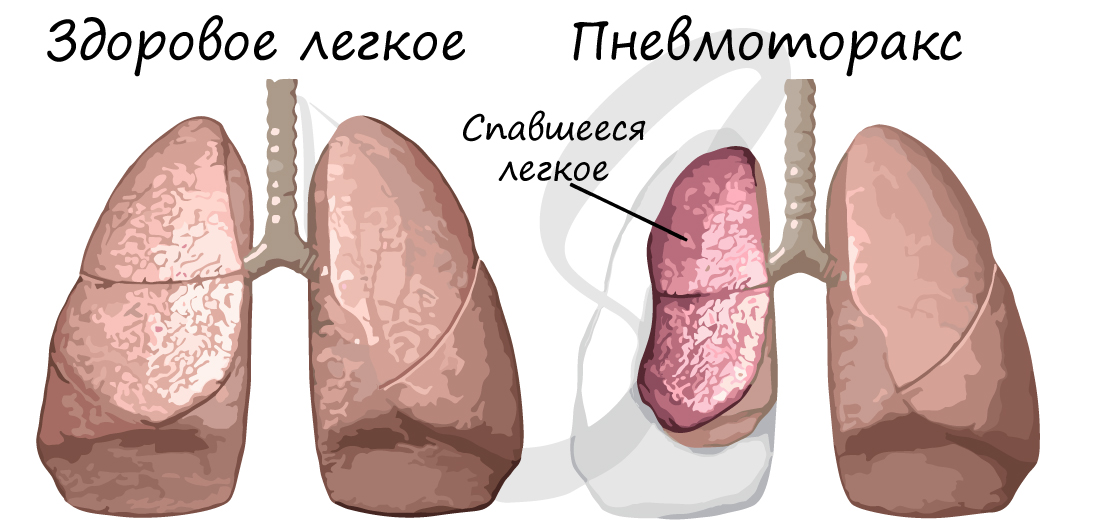
Пневмоторакс
В норме давление в плевральной полости отрицательное, оно обеспечивает растяжение легких. Однако при ранениях грудной клетки целостность плевральной полости может нарушаться: в таком случае давление в полости становится равным атмосферному.
Горная и кессонная болезни
Поначалу горная болезнь проявляется эйфорией (беспричинной радостью) и учащением пульса. Если покорение горных вершин продолжается, то к этим симптомам постепенно присоединяется апатия (состояние равнодушия), мышечная слабость, судороги и головная боль.
При резком быстром подъеме растворимость азота в крови понижается, и кровь буквально вскипает. Только представьте, в сосудах возникают настоящие пузыри газа! Они могут закупорить сосуды легких, сердца, других внутренних органов, в результате чего кровообращение остановится, и последствия могут быть самыми печальными, вплоть до летального исхода.
Как же предупредить кессонную болезнь? Можно использовать в дыхательной смеси вместо азота газ гелий, который не приводит к таким последствиям. Также необходимо придерживаться правила постепенного подъема, с остановками, избегать резкого всплытия.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Патологическая анатомия легких при новой коронавирусной инфекции (COVID-19). Предварительный анализ аутопсийных исследований
Полный текст
Аннотация
Обоснование. В настоящее время углубленно изучаются вопросы пато- и морфогенеза новой коронавирусной инфекции (COVID-19). Актуально проведение сравнительного анализа морфологических изменений легких умерших пациентов в различные временные сроки после появления первых клинических симптомов заболевания. Клинико-морфологические сопоставления должны способствовать повышению квалифицированной медицинской помощи пациентам реанимационного профиля и снижению больничной летальности.
Цель исследования — сформировать рабочую гипотезу концептуальной схемы клинико-морфологических фаз развития COVID-19 интерстициальной пневмонии на основе проведенных аутопсийных исследований.
Методы. Проведен анализ 80 летально закончившихся случаев в COVID-центре ФГБУ ФНКЦ ФМБА России. Наряду с оценкой макро- и микроскопических изменений респираторного тракта применена дополнительная гистохимическая окраска по Ван Гизону и выполнены иммуногистохимические исследования, позволяющие оценить состояние легких при COVID-19.
Результаты. Обнаруженные особенности диффузного альвеолярного повреждения при новой коронавирусной инфекции (COVID-19) позволили представить рабочую гипотезу патоморфогенеза COVID-19 интерстициальной пневмонии. Мы предлагаем три фазы — фульминантную, персистирующую и фибротическую, каждая из которых условно ограничена определенными временными параметрами и характеризуется определенными морфологическими признаками. Дисрегуляторная активация моноцитарных фагоцитов, развитие генерализованного тромбоза микроциркуляторного русла, патологическая репарация, прогрессирующий внутриальвеолярный и интерстициальный фиброз — основные звенья патоморфогенеза COVID-19-интерстициальной пневмонии. В ответ на внедрение вируса SARS-CoV-2 в экссудативной и пролиферативной стадиях преобладают реакции Т-клеточного иммунитета. В фибротической стадии общее количество Т-лимфоцитов резко снижено, клеток гуморального иммунитета не выявлено. Превалирование CD8+ Т-лимфоцитов-супрессоров над CD4+ Т-лимфоцитами-хелперами, возможно, связано с механизмами аутоиммунного поражения.
Заключение. Поражение легких с развитием COVID-19-интерстициальной пневмонии — основная причина тяжелого течения заболевания и летальных исходов. Выявленные особенности патоморфогенеза клинико-морфологических фаз COVID-19-интерстициальной пневмонии позволят улучшить качество диагностики и лечения новой коронавирусной инфекции (COVID-19).
Ключевые слова
Полный текст
ОБОСНОВАНИЕ
Новая коронавирусная инфекция (COVID-19) — потенциально опасное острое респираторное заболевание, вызванное новым коронавирусом (SARS-CoV-2), преимущественно с аспирационным механизмом передачи. В соответствии с санитарным законодательством Российской Федерации, вирус SARS-CoV-2 отнесен ко II группе патогенности [1]. COVID-19 может протекать не только в виде легкой острой респираторной вирусной инфекции, но и в тяжелых формах, которые характеризуются развитием клинической картины острого респираторного дистресс-синдрома (ОРДС) и полиорганной недостаточности с высокой летальностью [2, 3].
На протяжении периода пандемии пополняются научные сведения об этиологии, эпидемиологии, патогенезе и морфологических изменениях, клинических особенностях, лечении и профилактике новой коронавирусной инфекции [4–7].
Распространение COVID-19 представляет особую опасность в отношении декомпенсации хронических заболеваний. Наиболее часто тяжелые формы COVID-19 наблюдаются у пациентов с хронической обструктивной болезнью легких, ожирением, сахарным диабетом, артериальной гипертензией, ишемической болезнью сердца, хроническими заболеваниями почек, злокачественными новообразованиями [8–11].
Патогенез COVID-19 находится в процессе активного изучения. В отечественной и зарубежной литературе констатировано, что основным рецептором клеток, с которым связывается S-белок (Spike Protein) оболочки SARS-CoV-2, является ангиотензинпревращающий фермент 2 (angiotensin-converting enzyme 2, ACE2). Инфицирование происходит при участии трансмембранной сериновой протеазы 2 (transmembrane protease serine 2, TMPRSS2), необходимой для активации S-белка [12–15].
Рецептор ACE2 обнаружен на клетках различных органов (легкие, сердце, почки, тонкая кишка и др.), в том числе он присутствует на клетках иммунной системы, эндотелиальных клетках артериальных и венозных сосудов [16–19].
Основной мишенью вируса SARS-CoV-2 является респираторный тракт. Происходит поражение альвеолоцитов 1-го и 2-го типов, клеток эндотелия сосудов, что приводит к нарушению функционирования аэрогематического барьера и сурфактантного альвеолярного комплекса [15, 16].
Одной из наиболее актуальных патогенетических концепций COVID-19 является иммунная дисфункция (дисрегуляция), в основе которой лежит синдром активации макрофагов (macrophage activation syndrome, MAS) [16, 20, 21].
Дисрегуляторная активация моноцитарных фагоцитов, наблюдаемая у пациентов с тяжелыми формами COVID-19, возможно, ассоциируется с гипериммунным ответом, стимулирующим моноцитарно-макрофагальную систему легких с массивным выбросом цитокинов [16, 22, 23].
При генерализации инфекционного процесса наблюдается высокая продукция провоспалительных цитокинов и хемокинов с развитием «цитокинового шторма». Тяжелое течение COVID-19 сопровождается наиболее высоким уровнем в сыворотке крови интерлейкинов (interleukin, IL) 6, 8, 18, 1β и фактора некроза опухоли альфа (tumor necrosis factor-alpha, TNFα). Риск летального исхода ассоциирован с высоким уровнем IL6 в сыворотке крови [24, 25]. Гиперергическая иммунная реакция лежит в основе развития ОРДС и полиорганной недостаточности при COVID-19 [22].
Один из предполагаемых механизмов гибели клеток, инфицированных SARS-CoV-2, — пироптоз (вид программируемой некротической гибели клетки, при котором в результате активации каспазы 1 происходит нарушение целостности плазматической мембраны с формированием пор и быстрое высвобождение наружу содержимого клетки) [26, 27]. В очагах воспаления (внутриальвеолярно и в интерстиции) активированные макрофаги кроме выработки медиаторов воспаления секретируют ростовые факторы, запускающие процесс репарации и активирующие фибробласты.
В патогенезе ранних изменений важную роль играют активированные нейтрофилы, реагируя на любое нарушение гомеостаза в органах дыхания. Активация нейтрофилов способствует повреждению эндотелия, ухудшению реологических свойств крови, активации тромбоцитов и нарушению микроциркуляции. Объем и степень поражения микроциркуляторного русла напрямую коррелируют с течением и прогнозом заболевания [20]. Активированные нейтрофилы выделяют фактор активации тромбоцитов, обусловливая тем самым агрегацию и секвестрацию тромбоцитов, синтез фактора роста тромбоцитов, стимулирующего процессы фиброзирования.
Система мононуклеарных фагоцитов легких сопоставима с системой мононуклеарных фагоцитов печени, а диффузно развивающийся фиброз ткани легкого в исходе ОРДС при COVID-19 по своему течению целесообразно сравнить с отдельными формами вирусных поражений паренхимы печени (например, при вирусных гепатитах с исходом в цирроз печени). Не исключается возможность распространения (персистенции) коронавируса SARS-CoV-2 в организме за счет инфицирования клеток иммунной системы, более вероятно, макрофагов [28].
Морфологические признаки COVID-19 на современном этапе сводятся в основном к описанию изменений ранней (экссудативной) и поздней (пролиферативной) стадий ОРДС. Также верифицируется повреждение эндотелиоцитов микроциркуляторного русла с нарушениями в системе свертывания крови, развитием ДВС-синдрома с мультифокальным микротромбозом и последующей полиорганной дисфункцией с преобладанием острой почечной недостаточности [2, 3, 29].
Некоторые специалисты считают, что в отношении определения поражения легких при COVID-19 термин «пневмония» совершенно не отражает морфологию, клинико-рентгенологические признаки патологического процесса, наблюдаемого при поражении легких вирусом SARS-CoV-2. Предлагается к использованию термин «вирусное поражение легких» (вирусный пневмонит, вирусная интерстициопатия) [30]. Ряд авторов в качестве нового названия тяжелой COVID-19 предлагает термин «микрососудистый обструктивный тромбовоспалительный синдром легких» [31].
Звенья патогенеза и морфологические особенности новой коронавирусной инфекции требуют дальнейшего комплексного изучения с применением современных методов исследований. Остаются актуальными также вопросы правильного учета летально закончившихся случаев и эпидемиологической безопасности при проведении патологоанатомических вскрытий.
Цель исследования — изучить патоморфогенез COVID-19 на основе проведенных аутопсийных исследований с формированием рабочей гипотезы концептуальной схемы клинико-морфологических фаз развития заболевания.
МЕТОДЫ
Условия проведения
Проведено комплексное патологоанатомическое исследование секционного материала, полученного после аутопсий 80 умерших пациентов в ФГБУ ФНКЦ ФМБА России с основным заболеванием COVID-19 тяжелого клинического течения, подтвержденным выявлением методом полимеразной цепной реакции как при жизни, так и посмертно РНК SARS-CoV-2.
Характеристика (градация) исследуемых групп
Учитывая широкий спектр обнаруженных морфологических изменений в легких, в основе которых лежит диффузное альвеолярное повреждение, градация исследуемых групп проведена в соответствии с тремя стадиями ОРДС — экссудативной, пролиферативной и фибротической.
Первая исследуемая группа составила 12 случаев летальных исходов в течение 10 сут от начала клинических признаков COVID-19, вторая — 28 случаев, от 11 до 20 сут, третья — 40 случаев, от 21 до 45 сут.
Во всех случаях были выполнены патологоанатомические вскрытия с соблюдением временных методических рекомендаций по исследованию умерших с подозрением на новую коронавирусную инфекцию [29].
Методы исследования
Для исследования аутопсийного материала применялись гистологические, гистохимические и иммуногистохимические методы. Фрагменты трахеи, крупных бронхов, легких и внутренних органов фиксировали в формалине не менее 72 ч, далее проводили заливку в парафин. Серийные парафиновые срезы окрашивали гематоксилином и эозином, пикрофуксином по Ван Гизону. Из парафиновых блоков изготавливали срезы толщиной 3 мкм, которые окрашивали общепринятыми методиками.
В 13 случаях были выполнены иммуногистохимические исследования с антителами к СD3, CD4, CD8, CD20, CD31 (PECAM-1), CD34, СD57, CD68, CD138, Cytokeratin 5 & 6, гладкомышечному актину (actin, smooth muscle), сурфактантассоциированному белку А (surfactant A), коллагену IV типа (collagen type IV). Депарафинирование, регидратацию, демаскировку и окраску антигенов производили при помощи специализированной автоматизированной системы BenchMark® ULTRA (Ventana, США).
Статистический анализ
Результаты патологоанатомических исследований представлены в предварительном виде, так как набор и исследование материала продолжаются. Статистическая обработка будет выполнена позднее на большем объеме наблюдений.
РЕЗУЛЬТАТЫ
Основные результаты исследования
При аутопсийном макроскопическом и последующем гистологическом исследовании трахеи и легких пациентов, погибших от новой коронавирусной инфекции, были обнаружены морфологические признаки, отличающие ее от других острых респираторных вирусных инфекций.
Особенность макроскопической картины трахеи — неравномерность геморрагических изменений слизистой оболочки, которые чаще отсутствовали или минимально проявлялись в проксимальной части и были умеренно/резко выражены в дистальной части и главных бронхах.
При гистологическом исследовании дистальных отделов трахеи и бронхов крупного и среднего калибров были выявлены процессы нарушения кровообращения в сосудах микроциркуляторного русла подслизистого слоя в виде микроангиопатии (эритроцитарные сладжы, стазы, формирующиеся тромбы, периваскулярный отек). Нарушения кровообращения синхронно развивались с процессами повреждения, десквамации, очаговой базальноклеточной гиперплазии респираторного эпителия (рис. 1) с формированием фокусов плоскоклеточной метаплазии. Активные метапластические процессы, возможно, индуцированные вирусом, усугубляют течение инфекционного процесса, благоприятствуя распространению возбудителя, и нарушают мукоцилиарный клиренс, приводя к снижению барьерной функции эпителия.
Рис. 1. Базальноклеточная гиперплазия эпителия трахеи. Окраска гематоксилином и эозином, ×100
В 12 случаях летального исхода в течение 10 сут от начала заболевания макроскопически легкие были увеличены, тяжелые, тестоватой или плотной консистенции, маловоздушные, на разрезе с обширными участками «лакированного» вида, темно-красного (вишневого) цвета (рис. 2, А, Б). Присутствовали участки неравномерной окраски с чередованием сероватых, светло-багровых очагов, резко выраженного отека. В 5 случаях (смерть от 7 до 10 сут от начала заболевания) также отмечались единичные очаги зернистого вида, серовато-желтого цвета, и четко определялись участки геморрагических инфарктов правильной треугольной формы (рис. 2, В, Г) с наличием обтурирующих тромбов в сегментарных и субсегментарных ветвях легочных артерий.
Рис. 2. Макроскопическая картина легких при фульминантной фазе COVID-19-интерстициальной пневмонии, 9–10-й дни болезни
Примечание. A, Б — легкие «лакированного» вида на разрезе; В — участок геморрагического инфаркта легкого; Г — геморрагические инфаркты легкого на разрезе.
При гистологическом исследовании во всех случаях обнаружены основные морфологические признаки диффузного альвеолярного повреждения. Массивная гибель альвеолоцитов 1-го типа и синхронное поражение эндотелия капилляров приводят к экссудации жидкости и белковых молекул во внутриальвеолярное пространство, развитию отека легких, представленного серозным экссудатом, с присоединением преципитатов и нитей фибрина в просветах альвеол (рис. 3, схематическое изображение 1). По контурам альвеолярных ходов, альвеолярных мешочков, альвеол и части бронхиол формируются гиалиновые мембраны в виде полосовидных гомогенных эозинофильных масс (рис. 3, схематическое изображение 2). Погибшие альвеолоциты 1-го типа начинают компенсаторно замещаться пролиферирующими альвеолоцитами 2-го типа. Происходит денудация — «оголение» базальных мембран аэрогематического барьера (рис. 3, схематическое изображение 3–4) с разрушением его «рабочей зоны».
Рис. 3. Патоморфологические фазы COVID-19-интерстициальной пневмонии, соответствующие экссудативной (1–5) и пролиферативной (6–9) стадиям острого респираторного дистресс-синдрома (обозначения 1–9 приведены в тексте) [иллюстрация Ф.Г. Забозлаева]
В альвеолах среди фрагментированных гиалиновых мембран наблюдаются диффузно расположенные клеточные инфильтраты из легочных макрофагов (в том числе с формированием полинуклеарных форм), полиморфно-ядерных лейкоцитов, немногочисленных лимфоцитов, которые располагаются по типу «опавших листьев». Полиморфно-ядерные лейкоциты локализуются преимущественно вдоль межальвеолярных перегородок, в которых выявляются признаки нарушения микроциркуляции в виде эритроцитарных сладжей, стазов, фокусов экстравазации и дилатации капилляров (рис. 4).
Рис. 4. Микроскопическая картина альвеол при фульминантной фазе COVID-19-интерстициальной пневмонии. Окраска гематоксилином и эозином, ×100
Примечание. А — внутриальвеолярный отек с процессами его резорбции; стазы в мелких капиллярах межальвеолярных перегородок; Б — сформированные гиалиновые мембраны; интерстициальный отек межальвеолярных перегородок со слабовыраженной круглоклеточной инфильтрацией; В — пролиферация альвеолоцитов 2-го типа с их десквамацией и денудацией базальной мембраны; десквамированные альвеолоциты и легочные макрофаги в просвете альвеол; выраженный интерстициальный отек.
В просветах ветвей легочных артерий — фибриновые и эритроцитарно-фибриновые тромбы. Эндотелий в зонах прикрепления тромботических масс реактивно изменен: с признаками внутриклеточного отека, набухания, укрупненными ядрами. Также имеет место отек субэндотелиального слоя с гиперплазией мышечных клеток медиального слоя. Периваскулярная воспалительно-клеточная реакция во всех случаях выражена слабо, представлена скоплениями лимфоидных клеток и макрофагов. Вместе с тем определяются посткапиллярные венулиты с диффузной лимфолейкоцитарной инфильтрацией (рис. 5).
Рис. 5. Патоморфологические изменения в сосудах легких при фульминантной фазе COVID-19-интерстициальной пневмонии. Окраска гематоксилином и эозином
Примечание. А — фибриново-эритроцитарный тромб в мелкой ветви легочной артерии, ×40; Б — отек субэндотелиального слоя с гиперплазией мышечных клеток медиального слоя; периваскулярная воспалительно-клеточная реакция, ×100; В — посткапиллярный венулит с диффузной лимфоидной инфильтрацией, ×200.
При развитии геморрагического инфаркта из бронхиальной артерии поступает кровь, которая разрывает капилляры и изливается в просвет альвеол (рис. 3, схематическое изображение 5).
Проведено иммуногистохимическое исследование секционного материала 3 пациентов, умерших в течение 10 сут от начала заболевания. Во всех случаях обнаружено преобладание CD3+ Т-лимфоцитов над CD20+ В-лимфоцитами, CD4+ Т-хелперы превалируют над CD8+ Т-супрессорами (рис. 6, А, Б). CD20+ В-лимфоциты, CD57+ NK-клетки, CD138+ плазматические клетки немногочисленны, располагаются преимущественно в виде редких периваскулярных и перибронхиальных скоплений. Позитивная экспрессия антигена CD68 подтверждала наличие большого количества легочных макрофагов, расположенных преимущественно в просветах альвеол (рис. 6, В). Также высокая экспрессия CD31 (PECAM-1) документировалась в эндотелии кровеносных и лимфатических сосудов, макрофагах, гранулоцитах, при этом в данной стадии пролиферации кровеносных и лимфатических сосудов не выявлено (рис. 6, Г).
Рис. 6. Иммуногистохимический анализ изменений легких при фульминантной фазе COVID-19-интерстициальной пневмонии
Примечание. А — экспрессия CD4 Т-лимфоцитами-хелперами, ×100; Б — экспрессия CD8 Т-лимфоцитами-супрессорами, ×100; В — экспрессия CD68, ×100; Г — экспрессия CD31 (PECAM-1), ×200.
При оценке экспрессии сурфактантассоциированного белка А отмечены его гиперпродукция пролиферирующими альвеолоцитами 2-го типа и фагоцитоз легочными макрофагами, которые, заполняя просветы альвеол, входят в состав экссудата, состоящего из погибших альвеоцитов 1-го типа, лизированных эритроцитов, фибрина. Происходит дополнительный перфузионный блок к образованным гиалиновым мембранам, что препятствует газообмену в альвеолах.
Экспрессия коллагена IV типа обнаружена в участках деформированных «оголенных» базальных мембран аэрогематического барьера без накопления данного маркера в межальвеолярных перегородках.
При макроскопическом исследовании легкие 28 умерших пациентов второй группы (11–20-е сут) были увеличены, более плотной консистенции, мало- или безвоздушные. На разрезе отмечались участки «мозаичного» вида в виде резко выраженной гиперемии, распространенных сливных и очаговых кровоизлияний в сочетании с желтовато-розовыми и серовато-белесоватыми участками. В 19 случаях определялись геморрагические инфаркты (с диффузной локализацией в сегментах легких) при наличии в ветвях легочных артерий обтурирующих белесоватых и темно-красных тромбов. В целом морфологическая картина легких на разрезе напоминала порфировидный гранит, что позволило нам образно называть их «порфировые легкие» (рис. 7, А). Также имели место кровоизлияния в висцеральной и париетальной плевре. Наряду с вышеописанными макроскопическими признаками с большим постоянством встречались в отдельных сегментах персистирующие участки слабо-/умеренно выраженного отека, зоны «лакированного» вида. В 16 случаях наблюдались очаги зернистого вида вследствие присоединения вторичной бактериальной инфекции. В субплевральных отделах верифицировались различной протяженности и топографии белесоватые участки фиброза с формированием ретикулярного/сетчатого рисунка сероватого цвета.
Рис. 7. Макро- и микроскопическая картина легких при персистирующей фазе COVID-19-интерстициальной пневмонии, 18-й день болезни. Окраска гематоксилином и эозином, ×100 (Б, В, Д, Е); окраска по Ван Гизону, ×100 (Г)
Примечание. А — «порфировое» легкое; Б — участки деформированной альвеолярной паренхимы с гиалиновыми мембранами, врастанием грануляционной ткани в респираторные бронхиолы, альвеолярные ходы и альвеолы; В — внутриальвеолярный отек, макрофаги и десквамированные альвеолоциты с формированием мультинуклеарных структур, моноциты; Г — слабо-/умеренно выраженный периваскулярный фиброз; Д, Е — гиперплазия альвеолярного и бронхиолярного эпителия с участками плоскоклеточной метаплазии и реактивной дисплазии.
При гистологическом исследовании во всех случаях имеет место персистирование морфологических признаков экссудативной стадии диффузного альвеолярного повреждения с наличием внутриальвеолярного и интерстициального отека и формированием вновь образованных гиалиновых мембран. Вместе с тем наблюдается врастание грануляционной ткани в респираторные бронхиолы, альвеолярные ходы и альвеолы (рис. 3, схематическое изображение 8–9; рис. 7, Б). Синхронно определяются участки структурной перестройки архитектоники паренхимы легкого — зоны ателектазов и дистелектазов с компенсаторным расширением прилежащих альвеол и терминальных бронхиол. Просветы большинства альвеол щелевидной формы. В просветах альвеол определяются макрофаги, часть из которых с пенистой цитоплазмой, кариомегалией и формированием мультинуклеарных структур, клетки десквамированного альвеолярного эпителия, сливающегося в поликарионы, лимфоидные клетки и полиморфно-ядерные лейкоциты.
В интерстиции многочисленные фокусы сосудистой пролиферации, участки грануляционной ткани. Во всех случаях межальвеолярные перегородки деформированы и утолщены за счет разрастания коллагеновых волокон и воспалительно-клеточной инфильтрации, представленной макрофагами, лимфоидными клетками, полиморфно-ядерными лейкоцитами. Выявлен слабо-/умеренно выраженный периваскулярный фиброз (рис. 7, В, Г).
Отмечается гиперплазия бронхиолярного эпителия с участками плоскоклеточной метаплазии и реактивной дисплазии (рис. 3, схематическое изображение 6–7; рис. 7, Д, Е). Также имеет место смещение границ бронхоальвеолярного перехода в сторону альвеолярных ходов с бронхиолизацией альвеолярного эпителия. На фоне пролиферативных изменений отмечается массивная десквамация альвеолярного и бронхиолярного эпителия.
В случаях присоединения вторичной бактериальной инфекции в легочной паренхиме наблюдаются очаги острого воспаления вокруг бронхов или бронхиол размерами от ацинуса до сегмента. Воспалительная инфильтрация стенок бронхиол с накоплением преимущественно гнойного и смешанного экссудата в просветах альвеол, бронхиол и бронхов.
Проведено иммуногистохимическое исследование секционного материала 5 пациентов, умерших в течение 11–20 сут от начала заболевания. Во всех случаях обнаружено преобладание CD3+ Т-лимфоцитов над CD20+ В-лимфоцитами, при этом в 2 случаях пролиферативной фазы — превалирование цитотоксических CD8+ Т-супрессоров над CD4+ Т-хелперами (рис. 8, А, Б), в 3 случаях соотношение двух типов Т-лимфоцитов равное. Резко уменьшено количество CD20+ В-лимфоцитов, CD57+ NK-клеток по сравнению с экссудативной фазой. Плазматических клеток не обнаружено (реакция к CD138 отрицательная). Экспрессия антигена CD68 выявлена во всех случаях в большом количестве функционально активных макрофагов, расположенных преимущественно в просветах альвеол, меньше — в интерстиции межальвеолярных перегородок (рис. 8, В). CD31 (PECAM-1) экспрессируется в эндотелиальных клетках кровеносных сосудов, в том числе грануляционной ткани, малых лимфатических сосудов, также преимущественно в макрофагах (рис. 8, Г). При иммуногистохимическом исследовании с CD31 и CD34 выявлены признаки очагового повреждения эндотелия. Обнаружена положительная реакция к сурфактантассоциированному белку А, преимущественно в участках локализации альвеолярных макрофагов (рис. 8, Д).
Рис. 8. Иммуногистохимический анализ изменений легких при персистирующей фазе COVID-19-интерстициальной пневмонии
Примечание. А — экспрессия CD4 Т-лимфоцитами-хелперами, ×200; Б — экспрессия CD8 Т-лимфоцитами-супрессорами, ×200; В — экспрессия CD68, ×100; Г — экспрессия CD31 (PECAM-1), ×200; Д — экспрессия сурфактантассоциированного белка А, ×100.
У 40 пациентов, умерших в срок 21–45 сут от начала заболевания, легкие увеличены, безвоздушные. На висцеральной плевре — множественные кровоизлияния, реже формирование спаечного процесса. На разрезе паренхима легкого пестрого вида, с четкой градацией стадий диффузного альвеолярного повреждения, в отдельных случаях — с «этажностью» изменений. Преимущественно в верхних отделах легких — чередование зон резкого полнокровия, фокальных или массивных кровоизлияний, геморрагических инфарктов, синхронно сочетающихся с обширными участками фиброза, начинающегося преимущественно в субплевральных отделах и занимающего несколько сегментов в средних и нижних отделах обоих легких. В 14 случаях имели место признаки присоединившейся вторичной бактериальной инфекции. Паренхима легких в участках фиброза плотная, «каучуковой» консистенции, при суперинфекции — мелко- и крупнодольчатого строения. Прилежащая к участкам фиброза висцеральная плевра легкого с мелкобугристой поверхностью визуально напоминала капсулу цирротически измененной печени (рис. 9, А).
Рис. 9. Макро- и микроскопическая картина, иммуногистохимический анализ изменений легких при фибротической фазе COVID-19-интерстициальной пневмонии, 36-й день болезни. Окраска гематоксилином и эозином, ×100 (Б, Г–Е); окраска по Ван Гизону, ×100 (В)
Примечание. А — макропрепарат легких: прилежащая к участкам фиброза висцеральная плевра легкого с мелкобугристой поверхностью, визуально напоминает капсулу цирротически измененной печени; Б — пролиферативные, гиперпластические и метапластические изменения бронхиального и альвеолярного эпителия с формированием аденоматозных структур, очагов плоскоклеточной метаплазии с фокусами ороговения и реактивной дисплазии; В — диффузный фиброз легочной паренхимы при фибротической фазе COVID-19-интерстициальной пневмонии; Г — экспрессия гладкомышечного актина (actin, smooth muscle) пролиферирующих миофибробластов; Д — экспрессия Cytokeratin 5 & 6 в очагах плоскоклеточной метаплазии; Е — экспрессия коллагена IV типа.
При гистологическом исследовании — структурная дезорганизация паренхимы легкого с изменением нормальной гистоархитектоники за счет быстропрогрессирующего фиброза. Альвеолы преимущественно коллабированы (ателектазы и дистелектазы) с единичными щелевидными просветами (рис. 10, схематическое изображение 1–3). Межальвеолярные перегородки резко утолщены за счет отложения коллагеновых волокон с фокусами пролиферации фибробластов и миофибробластов, редукцией капиллярного русла, диффузной инфильтрацией макрофагами, полиморфно-ядерными лейкоцитами и немногочисленными лимфоцитами. Эпителиальная выстилка деформированных межальвеолярных перегородок представлена пролиферирующими альвеолоцитами 2-го типа, с признаками резко выраженных реактивных и дисрегенераторных изменений.
Рис. 10. Патоморфология фибротической фазы COVID-19-интерстициальной пневмонии
Примечание. ОРДС — острый респираторный дистресс-синдром [иллюстрация Ф.Г. Забозлаева]
Наблюдаются пролиферативные, гиперпластические и метапластические изменения бронхиального эпителия с формированием аденоматозных структур, очагов плоскоклеточной метаплазии с фокусами ороговения и реактивной дисплазии. В зонах аденоматозной гиперплазии — наползание метаплазированного бронхиолярного эпителия в просветы альвеолярных ходов (рис. 9, Б). Окрашивание по Ван Гизону выявляло на этой стадии диффузный фиброз легких (рис. 9, В).
Проведено иммуногистохимическое исследование секционного материала 5 пациентов, умерших в течение 21–45 сут от начала заболевания. Во всех случаях фибротической фазы обнаружено преобладание CD8+ Т-супрессоров над CD4+ Т-хелперами, при этом общее количество Т-лимфоцитов резко снижено. CD20+ В-лимфоциты, CD57+ NK- клетки не выявлены.
Положительная реакция к гладкомышечному актину (actin, smooth muscle) пролиферирующих миофибробластов и миофибробластических фокусов (рис. 9, Г). В участках плоскоклеточной метаплазии — положительная реакция к cytokeratin 5 & 6 (рис. 9, Д).
Резко выраженная экспрессия коллагена IV типа определяется по ходу утолщенных базальных мембран, в том числе сосудистого русла, бронхиального дерева, в интерстиции утолщенных и резко деформированных межальвеолярных перегородок (рис. 9, Е). На отдельных участках обнаружена более интенсивная реакция вокруг фокусов плоскоклеточной метаплазии.
ОБСУЖДЕНИЕ
Наш предварительный опыт патологоанатомических исследований умерших пациентов с тяжелыми формами полисегментарных, субтотальных и тотальных пневмоний, вызванных новым коронавирусом (SARS-CoV-2), в сочетании с обширной междисциплинарной информацией позволяет представить рабочую гипотезу патоморфогенеза COVID-19-интерстициальной пневмонии.
Острый респираторный дистресс-синдром при СOVID-19-интерстициальной пневмонии отличается от классической схемы развития диффузного альвеолярного повреждения, модифицированной в 2016 г. [32]. Согласно данной схеме, диффузное альвеолярное повреждение включает 2 стадии общей продолжительностью около 14 дней (рис. 11).
Рис. 11. Стадии острого респираторного дистресс-синдрома по Аnna-Luise A. Katzenstein, 2016 [32]
По нашему мнению, ОРДС при СOVID-19 имеет 3 стадии, которые сопровождают развитие соответствующих клинико-морфологических фаз COVID-19-интерстициальной пневмонии:
1) экссудативная стадия с развитием фульминантной фазы COVID-19-интерстициальной пневмонии;
2) пролиферативная стадия с развитием персистирующей фазы COVID-19-интерстициальной пневмонии;
3) фибротическая стадия с развитием фибротической фазы COVID-19-интерстициальной пневмонии.
Каждая стадия соответствует определенному времени развития заболевания и представлена характерными макро- и микроскопическими признаками (рис. 12).
Рис. 12. Стадии острого респираторного дистресс-синдрома, соответствующие фазам развития COVID-19-интерстициальной пневмонии
Экссудативная стадия соответствует острой фазе диффузного альвеолярного повреждения с развитием распространенного отека легких и формированием в последующем гиалиновых мембран (см. рис. 3), по протяженности занимает до 10 сут от начала клинических симптомов заболевания. Отличительная особенность экссудативной стадии — дисрегуляторная активация моноцитарных фагоцитов, вероятно, ассоциированная с гипериммунным ответом, стимулирующим моноцитарно-макрофагальную систему легких с последующим развитием микротромбоза в сосудах легких, при тяжелых формах — с генерализованным микротромбозом с поражением сосудов сердца, почек, головного мозга, верхних и нижних конечностей. При летальных исходах в течение экссудативной стадии мы посчитали необходимым указать на молниеносное течение соответствующей фульминантной фазы COVID-19-интерстициальной пневмонии.
Особенность пролиферативной стадии, которая составляет до 20 сут от начала клинических симптомов заболевания, — широкий спектр морфологических проявлений, постоянное сочетание персистирующих признаков экссудативной стадии в виде вновь появляющихся фокусов внутриальвеолярного отека и гиалиновых мембран с гиперпластическими, реактивными и дисрегенераторными изменениями, начальными признаками развития фиброза. Эти морфологические изменения позволяют говорить об атипическом течении ОРДС при новой коронавирусной инфекции (COVID-19). При этом непосредственные причины смерти наиболее часто связаны с тромбоэмболическими осложнениями и присоединением вторичной (бактериальной) инфекции.
При патологоанатомическом исследовании легких в фибротическую стадию (смерть от 21 до 45 сут и более от начала болезни) отмечалось субтотальное, но чаще тотальное поражение паренхимы с развитием диффузного интраальвеолярного и интерстициального фиброза при практически полном отсутствии функционально жизнеспособной легочной ткани. Примечательно, что интерстициальный фиброз, который в течение длительного времени развивается и сопровождает течение обычной интерстициальной пневмонии, а также фиброзный вариант неспецифической интерстициальной пневмонии, при фибротической фазе прогрессирующего тяжелого течения COVID-19-интерстициальной пневмонии формируется всего за 1,5–2 мес. Ранее данный признак мы также наблюдали при острой интерстициальной пневмонии (синдром Хаммена–Рича).
В случаях выживания пациентов с фибротической фазой COVID-19-интерстициальной пневмонии требуется квалифицированное катамнестическое наблюдение, поскольку можно прогнозировать их тяжелую инвалидизацию, требующую постоянной респираторной поддержки и рассмотрения вопроса о трансплантации легких вследствие высокой вероятности развития пневмоцирроза и опухолевой трансформации.
Проведенные в небольшом объеме иммуногистохимические исследования предварительно свидетельствуют, что в ответ на внедрение вируса SARS-CoV-2 преобладают реакции Т-клеточного иммунитета, который более выражен в экссудативной стадии с дальнейшим снижением. Превалирование CD8+ Т-лимфоцитов-супрессоров над CD4+ Т-лимфоцитами-хелперами при персистирующей и фибротической фазах коронавирусной (COVID-19) интерстициальной пневмонии может рассматриваться как признак вероятного аутоиммунного поражения.
Слабая выраженность реакций гуморального иммунитета при фульминантной фазе коронавирусной (COVID-19) интерстициальной пневмонии, отсутствие CD20+ В-лимфоцитов и плазматических клеток в фибротической стадии требуют дальнейшего изучения и клинико-морфологических сопоставлений.
Поражение легких с развитием COVID-19-интерстициальной пневмонии — основная причина тяжелого течения заболевания и летальных исходов. Выраженная воспалительная инфильтрация легочной ткани провоспалительными макрофагами, генерализованное поражение микроциркуляторного русла и более крупных сосудов с развитием тромбоэмболических осложнений, прогрессирующий фиброз паренхимы легких, присоединение вторичной бактериальной инфекции — предикторы неблагоприятного прогноза.
ВЫВОДЫ
ИСТОЧНИК ФИНАНСИРОВАНИЯ
Работа выполнена при финансовой поддержке ФМБА России.
КОНФЛИКТ ИНТЕРЕСОВ
Авторы данной статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
УЧАСТИЕ АВТОРОВ
Ф.Г. Забозлаев — написание статьи, методологическое обеспечение, общее руководство; Э.В. Кравченко — корректура статьи, подготовка иллюстративного материала, обработка дополнительных методов исследования; А.Р. Галлямова — анализ литературы, обработка морфологического материала; Н.Н. Летуновский — обработка иммуногистохимических исследований. Все авторы внесли существенный вклад в подготовку статьи, прочли и одобрили финальную версию до публикации.